仅供医学知识科普使用,请在医生指导下用药。

在代号为DESTINY-Gastric01的随机,II期,多中心,开放标签研究中,评估了DS-8201在HER2阳性晚期胃或胃食管交界处(GEJ)腺癌患者中的有效性。
关于DS8201
2023年12月7日,《OncLive》医学在线期刊公布了抗体偶联药物(ADC)德曲妥珠单抗(T-DXd,英文通用名:Enhertu,代号:DS-8201)治疗HER2低表达或阳性非小细胞肺癌(NSCLC)患者的疗效。这些患者伴有病理证实的软脑膜癌病。
此前,2019年12月,美FDA批准了德曲妥珠单抗上市,用于治疗接受过2种或以上抗HER2疗法的治疗的无法切除或转移性HER2阳性乳腺癌患者。
2022年5月5日,德曲妥珠单抗扩展适应症获美FDA批准,用于治疗无法切除或转移性HER2阳性乳腺癌患者,这些患者曾经接受过一种抗HER2靶向疗法的治疗。
2022年8月5日,德曲妥珠单抗新适应症获美FDA批准,用于治疗无法切除或转移性HER2低表达乳腺癌患者。
2023年2月24日,国家药监局(NMPA)官网最新公示,德曲妥珠单抗已在国内获批上市,用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。
2023年7月12日,德曲妥珠单抗获得国家药监局正式批准,用于治疗既往在转移性疾病阶段接受过至少一种系统治疗或在辅助化疗期间或完成辅助化疗之后6个月内复发、不可切除或转移性的HER2低表达成人乳腺癌患者。
德曲妥珠单抗由靶向HER2的人源化单克隆抗体通过四肽可裂解连接子与拓扑异构酶1抑制剂有效载荷连接组成。该药的作用机理为:首先通过药物中的抗体部分靶向并附着于癌细胞上的HER2;然后德曲妥珠单抗会进入癌细胞,释放化疗药物,ADC中的化疗部分可以杀死癌细胞以及附近的其它细胞。
2021年1月15日,FDA批准了fam-trastuzumab deruxtecan-nxki(Enhertu,DS-8201)用于治疗HER2阳性的局部晚期或转移性胃及胃食管交界处腺癌成年患者。
这是继HER2阳性晚期乳腺癌之后Enhertu的又一重磅适应症,展现了其在各类HER2阳性晚期癌症中的出色治疗潜力。此次批准基于Ⅱ期DESTINY-Gastric01试验(NCT04014075)的研究结果,该试验对比了曲妥珠单抗治疗后病情仍然进展的患者,接受Enhertu治疗或化疗的疗效。
根据最新公开的研究结果,Enhertu治疗患者的中位总生存期为12.5个月,而接受化疗(伊立替康或紫杉醇)的患者中位总生存期为8.4个月。
在缓解率方面,接受Enhertu治疗的患者整体缓解率为40.5%,显著高于接受化疗患者的11.3%;接受Enhertu治疗患者的中位无进展生存期为5.6个月,中位缓解持续时间11.3个月,同样显著超过了化疗患者的3.5个月和3.9个月。
2020ASCO:对于亚洲患者,临床疗效提升显著!
在2020年的ASCO大会上,研究者曾经公开了DESTINY-Gastric01试验的早期研究数据。此项试验中招募的患者基本来自亚洲,包括79.7%的日本患者的和10.3%的韩国患者。
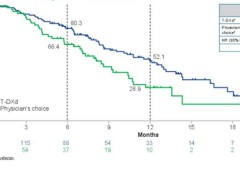
早期研究结果显示,接受Enhertu治疗的患者,整体缓解率达到了51.3%,显著超过了接受化疗(伊立替康或紫杉醇)患者的14.3%。
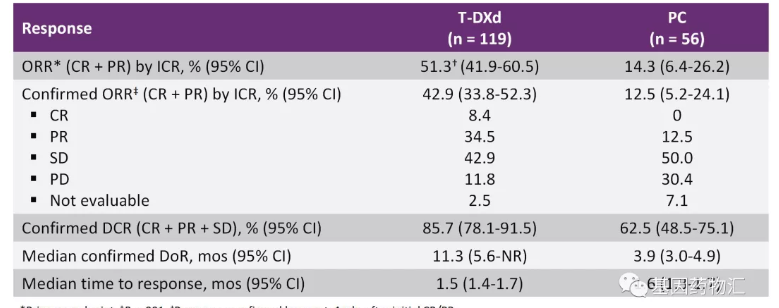
在生存期方面,Enhertu治疗患者的中位无进展生存期为5.6个月,中位总生存期为12.5个月,显著超过了化疗患者的3.5个月和8.4个月。

在不良反应方面,Enhertu治疗和化疗的患者最常见的不良事件均为嗜中性粒细胞减少(51% vs 24%),贫血(38% vs 23%)和白细胞计数减少(21% vs 11%)。
在接受Enhertu治疗的患者中,15.2%的患者因无法耐受而导致中止治疗,这一比例在接受化疗的患者中为6.5%;剂量限值性毒性在Enhertu治疗的患者中发生率为32.0%,在化疗患者中为33.9%。
随着分子靶向技术的发展,人们开始不再满足于化疗那“杀敌一千、自损八百”的“洗地式打击”,而是开始向着更精准的“靶向治疗”发展。但即使是能够精确靶向某一靶标的靶向治疗药物,在抗癌上也并非万能的。
被誉为“生物导弹的”抗体-药物偶联物(ADC)正是在这样的需求之下诞生的。
ADC通常由单克隆抗体、细胞毒性药物及两者之间的连接物共同构成。单克隆抗体具备“搜索”肿瘤的能力,能够精准靶向肿瘤病灶;在抵达病所之后,连接物断裂,释放细胞毒性药物,因此可以更加有针对性地提升病灶部位的药物浓度,将“好钢”用在“刀刃”上。
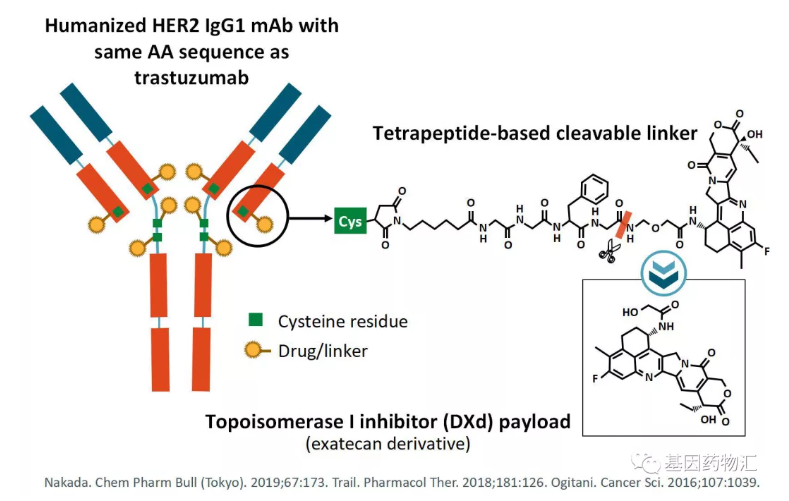
Enhertu,也称DS-8201,是一款非常具有代表性的经典ADC药物。它主要由能够精准识别并靶向HER2的单克隆抗体,以及化疗药伊立替康组成。
2019年底,Enhertu已经获得FDA批准用于治疗HER2阳性乳腺癌;此后2020年9月,Enhertu又于日本获批了胃癌的适应症。
除这两项适应症以外,Enhertu治疗非小细胞肺癌的DESTINY-Lung01试验也在进行中,目前得到的客观缓解率为61.9%,其中完全缓解率为2.4%,部分缓解率为59.5%;此外,还有28.6%的患者疾病稳定。
我们相信,以Enhertu作为“先遣队”,未来的临床上还会有更多的ADC药物登场,共同在抗癌这个“战场”上发挥力量。
为了帮助大家更好地熟悉抗癌药物、治疗癌症,基因药物汇为大家整理了正在免费招募胃癌患者的新药临床试验项目,为大家提供申请新药试验的途径。药物种类很多,大家可以先行咨询,后在医学顾问的指导下选择适合自己的新药。
符合标准的患者可以将基因检测报告、诊断报告的电子版或清晰照片发送至新药招募中心邮箱(doctor.huang@globecancer.com)进行申请,邮件中留下联系方式;或联系全球肿瘤医生网医学部(400-666-7998)进行详细咨询。
2. 备注【癌种】申请方舟援助金

患者咨询电话:400-666-7998

DS8201(trastuzumab deruxtecan,T-DXd) ,是一种HER2抗体+伊立替康类化疗药物的偶联药物,属于ADC型药物类型(抗体偶联药物)。它有两部分组成:第一部分是针对HER2靶点的抗体,可以精准的识别并且结合HER2高表达甚至低表达的肿瘤细胞;第二部分是剧毒的化疗药伊立替康。这种设计会使抗体带着化疗药去找肿瘤细胞,然后精准地给肿瘤细胞下毒,毒死它们。
这种药物设计结合了靶向药的精准和化疗药的高效,既避免了全身使用化疗药的毒副作用,也比单独使用靶向药具有更强的杀伤能力,一举两得。

全球肿瘤医生网不具备药品销售资格,不售卖任何药物,也不帮助患者代购药物。网上药品代购存在假药等风险,且代购均为违法行为,请广大患者做好自我保护。

适应症:预计FDA将基于DESTINY-Gastric01的惊艳数据,批准DS-8201作为胃癌晚期治疗的新药上市。...
厂家:暂无
美国价格: 暂无 香港价格: 暂无
规格:暂无
医保:无医保
是否上市:在研