


新码生物重组人源化抗HER2单抗-AS269偶联物(ARX788)HER2阳性乳腺癌临床试验II/III期招募整在进行中
根据国家药监局最新公示,浙江医药旗下子公司新码生物研发的注射用重组人源化抗HER2单抗-AS269偶联物(ARX788)已于5月25日结束公示,正式纳入突破性治疗品种目录,拟定适应症为HER2阳性晚期乳腺癌二线治疗。
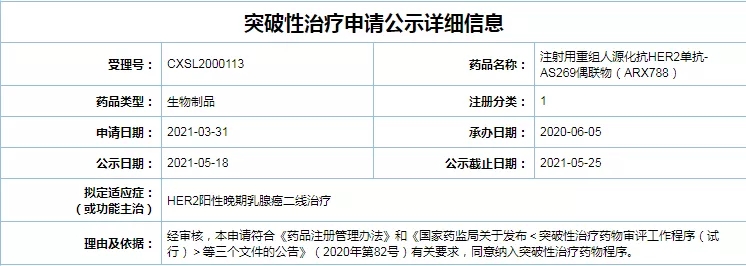
国家药监局官网
当前乳腺癌已成为全球发病率最高的癌症,其中HER2阳性约占全部乳腺癌的20%~25%,这类患者往往具有预后差、疾病易复发、生存期短的特点。目前,我国尚无抗HER2-ADC类药物在HER2阳性晚期乳腺癌二线治疗获批上市,巨大的临床需求有待填补。
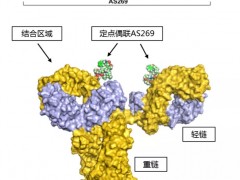
ARX788是新码生物与Ambrx共同开发的一款靶向HER2阳性肿瘤抗体药物偶联物(ADC)。该产品由2个细胞毒素分子AS269与曲妥珠单抗借助非天然氨基酸专利定点偶联技术制成,能够实现毒素在单抗分子上的精确偶联,从而实现更高的安全性及稳定性。
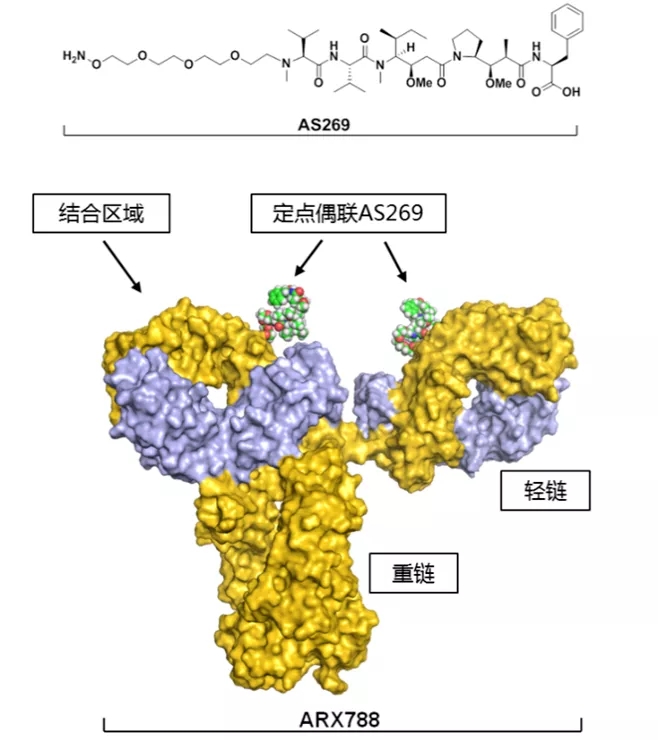
图片源自新码生物
目前,ARX788治疗HER2阳性晚期乳腺癌的Ⅰ期临床研究正在进行。根据新码生物公布的数据,截止2021年1月21日,69名患者中有33人达到客观缓解,总客观缓解率(ORR)为47.8%,其中1.5 mg/kg Q3W(II期推荐剂量)剂量组ORR为65.5%,并且患者接受治疗后的不良反应以轻中度为主,显示该产品具有良好的安全性。
据悉,ARX788针对乳腺癌和胃癌的II/III期临床研究已经相继启动,国内开发进度快于欧美。在美国,ARX788已获得FDA授予快速通道资格,用于治疗已接受过一种或多种抗HER2治疗的晚期或转移性HER2阳性乳腺癌,以及FDA授予孤儿药资格,治疗HER2阳性胃癌和胃食道结合部癌。
推荐阅读:
浙江医药ARX788临床试验,评价重组人源化抗HER2单抗-AS269抗体偶联药物(ARX788)治疗HER2阳性的晚期乳腺癌临床试验
内容太专业看不懂?没关系,点击在线咨询,在线客服会详细为您讲解招募相关情况,欢迎咨询!
参考资料:
[1]新码生物官网
[2]国家药监局官网
[3]http://www.myzaker.com/article/6024c9088e9f094e861decaf
[4]https://mp.weixin.qq.com/s/utnfO13QMye6ld5-fdRhuw
内容来源:林山月 生物探索
2. 备注【癌种】申请方舟援助计划


患者咨询电话:400-666-7998

全球肿瘤医生网提醒患者:国内细胞免疫治疗技术,包括cart细胞,树突细胞疫苗,NK细胞
TILs细胞,TCR t细胞治疗癌症疫苗等技术均处于临床试验阶段,未获准在医院正式使用。国内患者可以参加正规临床试验,在医生的监管下使用,全球肿瘤医生网不推荐患者贸然尝试任何医疗机构和研发机构的收费治疗。
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。

-

-
肿瘤电场疗法——被FDA批准治疗复发性胶质母细胞瘤等
目前电场疗法已被FDA批准用于治疗复发性胶质母细胞瘤、新诊断的胶质母细胞瘤以及恶性胸膜间皮瘤,并且在目前在六大实体肿瘤包括非小细胞肺癌 详细»
-

-
临床试验中心——每一个新药都是一份希望
提供癌症临床试验招募信息、抗肿瘤新药受试者招募信息。 详细»
-

-
10个值得关注的乳腺癌临床试验招募项目
这一次,基因药物汇为大家汇总了招募乳腺癌患者的3大类、10小项临床试验项目,申请方法列在文末的海报上,希望能够帮助到正在寻求新药治疗的患者。 详细»
-
-
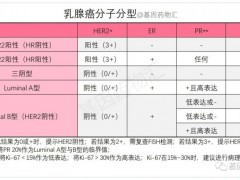
乳腺癌临床试验,乳腺癌不化疗的临床试验正在招募患者
从治疗的角度来说,乳腺癌的分子分型与治疗方案有非常密切的联系。 详细»
-

-
PARP抑制剂HTMC0435临床试验正在招募一线治疗失败的晚期乳腺癌患者
HTMC0435是一款PARP1/2抑制剂。根据目前的临床前研究结果,这款药物对于多类肿瘤、尤其是BRCA1/2突变的实体瘤有较好的治疗效果,最理想情况下可使肿瘤完全消退。 详细»
-

-
富龙康泰mTORC1/mTORC2双重抑制剂抑制剂FP-208临床试验正在招募经过治疗或无标准治疗方案的乳腺癌患者
FP-208是一款由北京富龙康泰研发的,基于新靶点、新机制的mTORC1/mTORC2双重抑制剂,拥有自主知识产权。 详细»
-
-
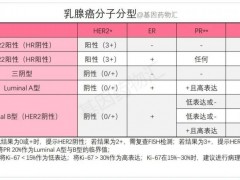
EGFR/HER2不可逆抑制剂AMX3009马来酸片临床试验正在招募HER2阳性的晚期乳腺癌患者
AMX-3009马来酸片是安润医药自主研发的一种EGFR/HER2不可逆抑制剂,其临床试验申请(化药1类)于2019年2月经国家药品监督管理局(NMPA)受理。 详细»
-

-
靶向联合免疫MRG002+HX008临床试验正在招募HER2低表达的晚期乳腺癌患者
这两款新药的组合,在HER2阳性以及HER2低表达的患者当中都具有一定的治疗潜力。 详细»
-
-
新码生物重组人源化抗HER2单抗-AS269偶联物(ARX788)HER2阳性乳腺癌临床试验II/III期招募整在进行中
ARX788是新码生物与Ambrx共同开发的一款靶向HER2阳性肿瘤抗体药物偶联物(ADC)。 详细»
-
-
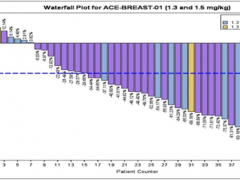
新码生物ARX788疗效数据媲美DS8201,HER2阳性乳腺癌临床试验招募进行中
新码生物ARX788疗效数据媲美DS8201,DCR高达100%! 详细»






























 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城