portant; word-wrap: break-word !important;">高级胶质瘤是一种致命的脑肿瘤,包括:成年胶质母细胞瘤,美国亚利桑那州参议院的约翰·麦凯恩罹患的就是这种脑癌; 间变性少突胶质细胞瘤;儿童胶质母细胞瘤; 和称为弥漫性内分泌神经胶质瘤的儿科肿瘤。五年生存率分别为:少突胶质细胞瘤60%,成人和儿科成胶质细胞瘤约占10%,而DIPG(脑干肿瘤)几乎为0。 迫切需要新的治疗方法。
portant; word-wrap: break-word !important;">全球肿瘤医生网为大家总结除化疗外的另一大治疗手段,靶向药物治疗在脑胶质瘤中的进展。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">
众所周知,贝伐珠单抗是目前脑胶质瘤FDA获批的靶向药物,它对无进展生存期的延长作用曾令医学界备受鼓舞,但随后其被证实在总生存期延长方面表现平平,未能延长总生存期。目前,贝伐珠联合化疗药物、病毒载体、放疗及与免疫药物对比的临床Ⅲ期正如火如荼的开展,我们拭目以待。

贝伐珠单抗相关Ⅲ期临床试验
在基因突变较少的儿童低级别胶质瘤中,MAPK信号通路是其主要的突变来源,BRAF基因是MAPK信号通路中的重要组分,在胶质瘤的发生发展中起重要作用。
2017年,加拿大的一项研究发现BRAF V600E突变的低级别儿童胶质瘤患者对常规放化疗不敏感,10年的无进展生存率(PFS)为27% ,而BRAF野生型PFS为60.2%。6名BRAF V600E突变的患者在常规治疗疾病进展后使用了BRAF抑制剂,SickKids组织和另一个国际组织使用化疗进行对照。经过6个月的治疗,化疗组有23%的患者对化疗响应(肿瘤组织缩小25%),有24%的患者疾病进展并使用了二线三线的化疗方案;而使用BRAF抑制剂的6名患者对治疗响应显著,肿瘤缩小49%到80%(如下图红框所示),这6名患者后续平均服药18.5个月,这期间疾病稳定。
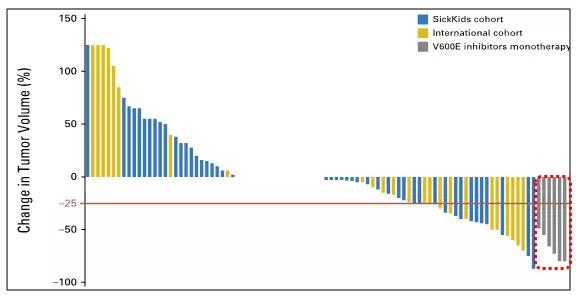
不同治疗方式下肿瘤响应程度比较
同时,BRAF继发耐药机制也取得一定进展。人胶质瘤模型研究发现,在维莫非尼治疗BRAF V600E突变的胶质瘤中,Axl和EGFR信号通路是导致靶药耐药的重要因素。EGFR和Axl抑制剂加强肿瘤细胞凋亡并抑制肿瘤的生长。因而,BRAF抑制剂联合特定的药物组合(如EGFR和Axl 抑制剂)可能会令BRAF V600E突变的胶质瘤患者最大获益。
儿童胶母中较常见的致癌基因融合约占10%,MET基因融合为其中的典型,下图左为MET基因融合的类型。MET融合激活MAPK信号通路,破坏细胞周期调控,诱导肿瘤进展。MET抑制剂的模型研究发现其能抑制MET突变的肿瘤生长。
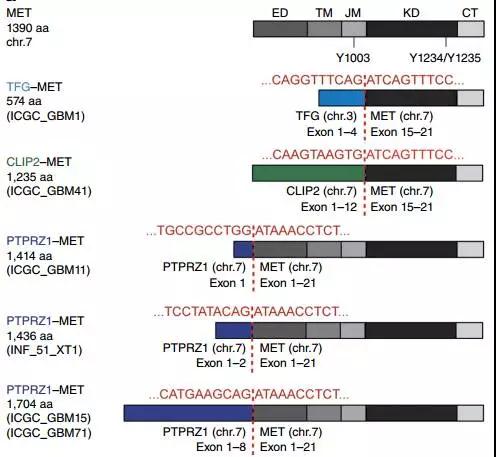

MET融合形式及MET抑制剂治疗效果
一名8岁的男孩,具有复发的小脑胶质母细胞瘤,伴随PTPRZ1-MET基因融合,使用MET抑制剂克唑替尼治疗后,11周内肿瘤显著减小(如右图上方长箭头所示),此位置症状缓解,但其他的位置发生新的耐药病灶(如右图下方三角箭头所示),由此可见综合治疗可能是达到持久临床获益的必经之路。
一项Ⅱ期临床试验结果表明,成人复发低级别胶质瘤使用mTOR抑制剂依维莫司后疾病较稳定,半年PFS为84%,一年PFS为47%。依维莫司的抗肿瘤作用还表现在肿瘤血管结构改变。以上结果支持依维莫司在低级别胶质瘤中做进一步探索。
临床前试验也有一批好结果,主要集中在多靶点联合用药和双靶点抑制剂上。
1
多靶点联合用药
CDK4/6 抑制剂帕布利昔布抑制mTOR下游信号通路活性,使mTOR信号通路激活。依维莫司抑制mTOR通路,激活Ras的介导子Erk,帕布利西布可结合抑制Erk。依维莫司与帕布利昔布组合治疗显著干扰了胶质母细胞瘤(GBM)的代谢,导致大量细胞凋亡,且依维莫司显著提高了帕布利昔布在脑中的浓度。CDK4/6与mTOR抑制剂对GBM有治疗潜力,建议开展临床试验进一步评估。
1
双靶点抑制剂
DS7423为PI3K/mTOR双靶点抑制剂, 在小鼠中能穿越血脑屏障。DS7432对PI3K通路激活且PTEN失活的胶母细胞系有抑制作用。NVP-BEZ235是 PI3K/mTOR 双靶点抑制剂, 能增强放疗对成人和儿童胶母细胞系中的杀伤作用并导致早期的肿瘤代谢改变,此变化通过核磁共振光谱呈现。
随着一代mTOR抑制剂雷帕霉素、二代mTOR抑制依维莫司等的涌现,耐药问题也随之而来,而三代mTOR抑制剂Rapalink-1的研究为耐药问题带来曙光。
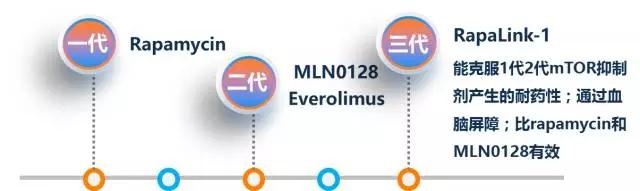
mTOR抑制剂发展进程
去年《Nature》上发表了Rapalink-1能克服一代和二代mTOR抑制剂产生的耐药性的研究结果,今年其在胶质母细胞瘤中研究表明,其能穿越血脑屏障对体内试验的三个模型起抑制作用,且比雷帕霉素和MLN0128的有效性强。期待三代 mTOR抑制剂尽快进入临床试验阶段,带来等多好消息。
EGFR类抑制剂,目前在Ⅱ期试验的药物有艾乐替尼、ABT-414、Sym004、PF-299804、阿法替尼、西妥昔单抗、Tesevatinib等(下图为部分试验)。

EGFR靶向药物相关临床Ⅱ期试验
一项Ⅲ期临床实验结果表明,新诊断的EGFRvIII表达的胶母患者使用Rindopepimut 生存期未延长。Rindopepimut对胶母患者的免疫疗效可能需要通过联合用药来实现。
除以上成熟的信号通路中的重要研究外,更多的有价值的靶点被科学家们带入了大众视野,如BCL6基因,BCL6是胶质母细胞瘤预后的标志物( BCL6过表达预后较差)及肿瘤发展的促进因子,BCL6基因沉默抑制GBM细胞生长引发细胞衰老,其是胶质母细胞瘤的潜在治疗靶点。又如EZH2基因, 研究发现EZH2抑制剂是潜在的H3K27M突变的儿童胶质瘤治疗方法。
综上所述
胶质瘤的靶向研究的重点从过去的单药的评估到联合治疗的评估、多靶点药物的开发及耐药机制和新一代耐药药物研发方向转移,无论是从基因层面挖掘新的靶点还是临床试验的应用研究都在日新月异改善着我们的医疗环境。让我们为改善患者的生活质量而共同努力,路漫漫其修远兮,吾将上下而求索!
推荐阅读:脑瘤基因检测








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城