两款BCMA CAR-T伊基奥仑赛和泽沃基奥仑赛长短期疗效对比
近年来,CAR-T细胞疗法在治疗血液系统恶性肿瘤方面取得了巨大的成功。中国已超越美国成为CAR-T细胞疗法临床研究的主要力量(1)。
在多发性骨髓瘤(MM)领域,已有2款全人源靶向BCMA CAR-T药品先后获得NMPA的正式批准用于治疗复发/难治性MM(R/R MM),分别是伊基奥仑赛和泽沃基奥仑赛。这2款药品疗效究竟如何?让我们从两个产品说明书中披露的中国人群大样本2期注册临床疗效数据来一起探究。
鉴于1期研究样本量小(往往<20)且剂量不统一,主要用于探索不同CAR-T剂量在人体中的安全性和耐受性,为2期临床研究设计做铺垫;而CAR-T药品的2期注册临床其数据用于CAR-T的上市申请,样本量必须足够(一般需>100例)、剂量和生产工艺必须保证和最终获批药品要求保持一致;因此,中国2期注册临床的结果能够客观展示一个已获批CAR-T药品在中国研究人群的疗效和安全性。
此处小编提示,两个产品的2期注册临床非头对头对比,且两者基线存在差异:泽沃基奥仑赛说明书中标注其注册临床研究中纳入了前次治疗后未进展(入组时疾病稳定)患者(7/102),而伊基奥仑赛注册临床入组患者均为复发或进展患者。
中国大样本注册临床:两款BCMA CAR-T短期疗效
从外周血中CAR-T细胞的中位达峰时间来看,伊基奥仑赛为12天,泽沃基奥仑赛为14天(2,3)。临床试验结果也似乎证实了这一结果,伊基奥仑赛的中位达缓解时间为15天,泽沃基奥仑赛的中位达缓解时间为29天(2,3)。
随访3个月时,两个产品说明书披露了中国大样本注册临床3个月的完全缓解(CR)率:伊基奥仑赛注册临床研究显示为40.3%,泽沃基奥仑赛注册临床研究显示为28.3%(2,3)。
还有一点值得注意,伊基奥仑赛输注剂量为1x10^6细胞/kg。泽沃基奥仑赛的输注总剂量为150x10^6细胞,按照70kg-75kg体重换算,其剂量是伊基奥仑赛剂量的2倍或更高(2,3)。同时泽沃基奥仑赛的回输剂量也不是固定的,且某些患者可能需要分两次复苏和回输。
中国大样本注册临床:看两款BCMA CAR-T长期疗效
从CAR-T细胞体内存续时间来看,伊基奥仑赛存续6个月的患者达62.3%,泽沃基奥仑赛存续6个月的患者为26.5%(2,3)。从已披露数据看,泽沃基奥仑赛的中位存续时间为77天(4);伊基奥仑赛的中位存续时间为419天(5)。
从两个BCMA CAR-T中国大样本注册临床结果来看,两者的长期疗效都体现出随着时间不断加深的趋势,同时在每个时间节点,因为存续能力的不同,也体现出疗效差异(图1)。
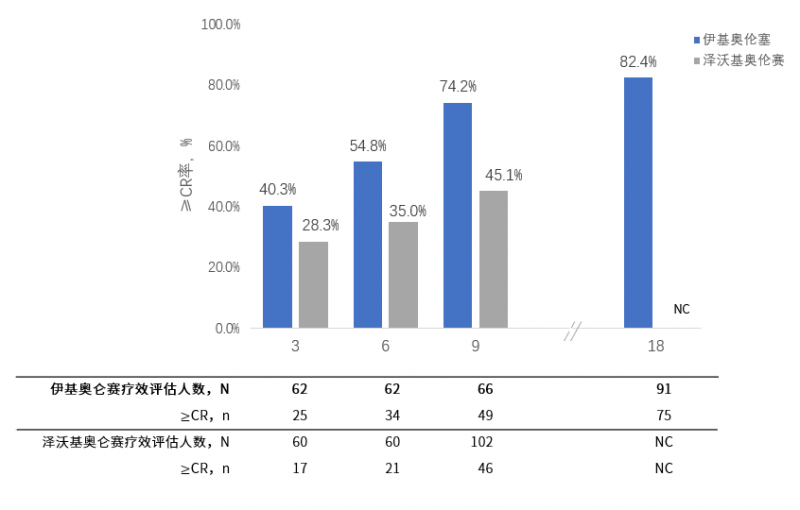
图1 不同随访时间节点中国大样本注册临床的≥CR率比较
NC:未披露
注:以上数据为自行整理,非头对头研究。
此处随访6个月时的CR率为两个产品说明书中分别披露的中国大样本注册临床数据:伊基奥仑赛为54.8%,泽沃基奥仑赛为35.0%(2,3)。
中位随访时间9个月左右时,两个产品在2022年EHA和ASH分别披露了中国大样本注册临床数据:伊基奥仑赛中位随访9.6个月≥CR率为74.2%(6),泽沃基奥仑赛在中位随访9个月时的≥CR率为45.1%(7)。
2023年IMS大会上,伊基奥仑赛披露了最新长期随访数据:中位随访时间达18.07个月时,其≥CR率进一步提高,达82.4%8。而泽沃基奥仑赛中国大样本注册临床数据既2022年底之后,尚未公开披露中位随访9个月之后的疗效数据。
本文以两个已获批BCMA CAR-T说明书中的中国大样本注册临床数据为标准,从药效及药代动力学角度试图探寻不同已上市CAR-T药品在中国人群的疗效和造成差异的原因;如有不足之处,欢迎批评指正。
参考文献:
[1] Hu Y, et al. Lancet Haematol. 2022;9(12):e930-e941.
[2] 伊基奥仑赛注射液说明书.
[3] 泽沃基奥仑赛注射液说明书.
[4] Blood (2022) 140 (Supplement 1):4564-4565.
[5] 2023 ASH. Poster 4854.
[6] Li, C. ,et al. HemaSphere 6():p 88-89, June 2022.
[7] 2022ASH. Poster 1994.
[8] 2023 IMS. P-290.








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城