两款血液肿瘤TCR-T疗法产品TSC-100和TSC-101,I期效果惊艳,实现零复发
据环球通讯社(Source: GlobeNewswire)报道,2024年2月26日,TScan Therapeutics生物制药公司,在ASTCT(即美国移植和细胞治疗学会)和CIBMTR(即国际血液和骨髓移植中心的移植和细胞治疗会议)串联会议上,公布了两款新的TCR-T疗法产品——TSC-100和TSC-101的Ⅰ期最新临床研究数据(NCT05473910),旨在治疗残留病灶并预防造血干细胞移植(HCT)后复发的急性髓性白血病(AML)、急性淋巴细胞白血病(ALL)、骨髓增生异常综合征(MDS)患者,目前该公司在积极探索2期临床试验推荐剂量。
既往TCR-T疗法的研发主要针对实体瘤,此次公布的这两款产品却对血液肿瘤重拳出击,为TCR-T疗法的研发及应用开辟了新的赛道!

▲截图源自“FINANCIAL TIMES”
TSC-100和TSC-101剑指血液肿瘤
大约30%~40%的急性髓性白血病(AML)患者,在异基因造血干细胞移植(HCT)治疗后复发,使得这类患者的治疗选择较为局限。
TSC-100和TSC-101是同种异体供体来源的T细胞受体基因工程改造的T细胞(TCR-T),分别靶向HA-1和HA-2造血细胞抗原,两者均呈递于HLA-A*02:01。该药通过选择HLA-A*02:01或HA-1阴性的供体,可选择性消除造血干细胞移植后,残留的患者造血细胞,并预防癌症复发(治病机理详见下图)。
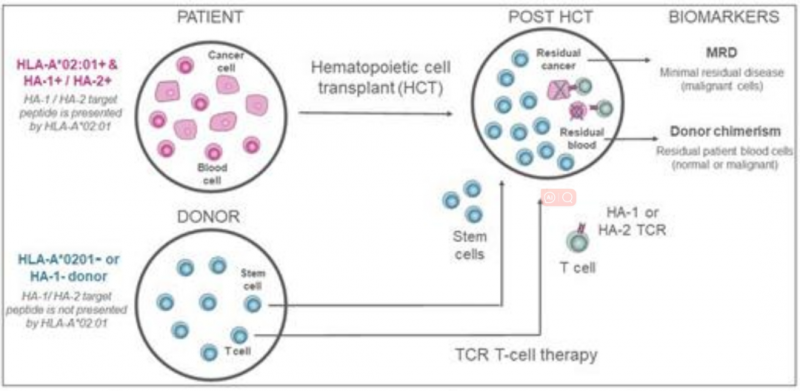
▲图源“Blood”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
TSCAN-001(NCT05473910)是一项多中心、多臂非随机、对照1期研究,目的是评估TSC-100和TSC-101的可行性、安全性和初步疗效。
将入组的患有AML、MDS或ALL的成年患者分为两组,即治疗组(HLA-A*02:01和HA-1/HA-2阳性患者)、对照组(HLA-A*02:01阴性患者)。入组后,治疗组(8例)患者先接受HCT治疗,再接受TSC-100(4例)或TSC-101(4例)治疗;对照组患者仅接受HCT治疗(3例)。HCT随访后中位时间为111天(范围33-266天)。结果显示如下:
1、TSC-100治疗组(N=4:T-ALL、AML、AML、MDS:接受TSC-100治疗的全部4例患者,均完全的供体嵌合,且没有复发。
2、TSC-101治疗组(N=4:TP53突变MDS、AML、B-ALL、B-ALL):接受TSC-101治疗的全部4例患者实现了完全供体嵌合,且没有复发。
其中包括1例患有高危TP53突变的MDS,在接受TSC-101治疗后,现已达到1年未复发的奇迹,具有里程碑氏的意义!因为随着时间的推移,复发的可能性显著降低,从而有助于改善生活质量。
此外,1例在HCT治疗后呈MRD阳性的AML患者,在TSC-101治疗后转为MRD阴性,并维持MRD阴性状态(最近一次测量是在第180天)。
TSC-100及TSC-101在给药后的所有监测时间点,均持续存在,且最长的随访时间超过9个月。此外,与单次给药(剂量水平1)相比,重复给药(剂量水平2和3)导致循环TSC-100和TSC-101水平增加3倍。
综上,造血干细胞移植后,使用TSC-100/101靶向MiHAHA-1或HA-2,显示出早期安全性和有效性的生物标志物证据,从而降低复发风险。
TCR-T疗法血液肿瘤招募进行时
目前正有两款研发的TCR-T疗法,在招募复发难治恶性血液病、复发/难治性EBV阳性淋巴瘤患者,想要参加的患者可以咨询医学部,了解详细的入排标准。
此外,若想寻求其他细胞疗法(如CAR-T、TILs、CAR-NK、CTL、NK)帮助的患者,同样可将治疗经历、病理报告、出院小结等,提交至医学部,初步评估病情。








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城