全新的KRAS TCR-T细胞疗法治疗胰腺癌,肿瘤缩小了72%
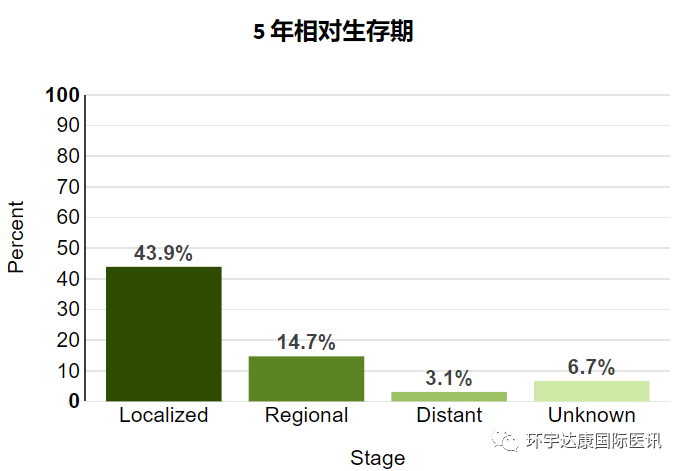
胰腺癌是最致命的癌症之一。因为晚期胰腺癌的五年生存率仅为3,1%,是所有常见癌症中最低的。更可怕的是,大部分患者在初始手术治疗时肝脏和其他部位就可能存在隐匿微转移,一旦复发,化疗的作用有限,预后很差,此外,近两年被誉为“神药”的PD-1在胰腺癌中也未达到理想效果。
为了早日攻克“癌王”,全球的医学家们都在积极探索各种治疗方案。终于有了一款新型的免疫疗法让“它”闻风丧胆,令经过大量治疗失败的晚期胰腺癌患者肿瘤缩小72%,并在2022年6月2日登上了国际顶级期刊《新英格兰医学杂志》,我们一起来来这是款什么样的新疗法。

胰腺癌消退72%!全新改造的TCR-T疗法曙光初现
这项研究之所以在医学界引起轰动,是因为一位接受了各种治疗失败的晚期胰腺癌患者,在接受了T 细胞受体 (TCR) 转导的,专门针对KRAS G12D突变的新型TCR-T疗法后,全身的转移病灶竟然消失了72%!给胰腺癌患者带来了新的曙光。
大约 90% 的胰腺癌存在 KRAS 突变,其中最常见的亚型就是KRAS G12D,占到了41%!基于这一具有特异性靶点的庞大患者群体,研究人员专门研发了靶向KRAS G12D的TCR-T疗法。
简单来说,TCR-T疗法需要从患者身上获取T细胞进行改造,让T细胞表达能够有效识别肿瘤细胞的TCR(T cell receptor,T细胞抗原受体)使其能够靶向特定的癌症抗原的疗法。这种新型的疗法可以允许医生为每个患者的肿瘤和不同类型的T细胞选择最合适的靶点进行工程改造,使治疗个体化,并为患者提供更大的缓解希望。
在这项实验中,研究人员将胰腺癌患者的T细胞在体外进行基因工程改造,使其表达两种不同的TCR,TCR能够识别被癌细胞的HLA蛋白呈递在癌细胞表面的肿瘤抗原。这两种TCR不仅能够精准识别包含KRAS G12D突变的多肽,而且不会对野生型的KRAS产生反应,从而能够精准靶向癌细胞。
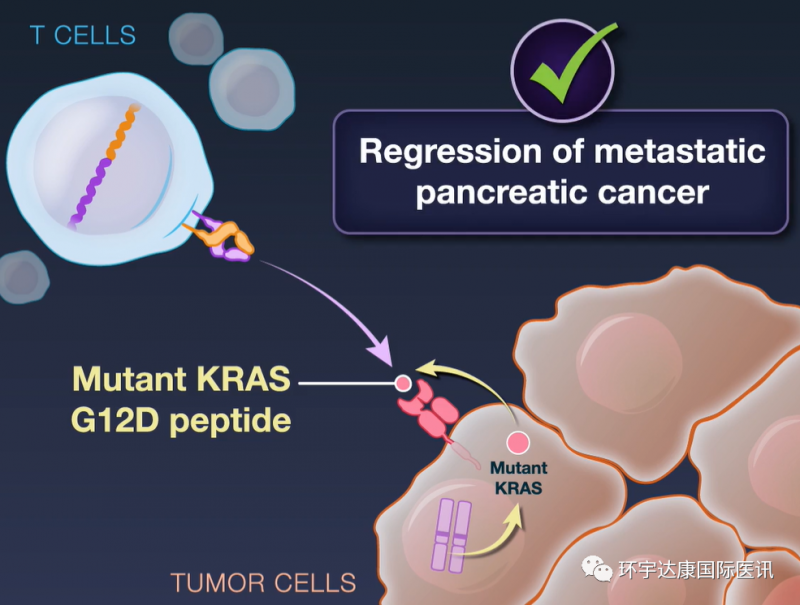
实验结果也非常振奋人心。67岁的M女士成为这一疗法的首位获益者。
2018年,M女士确诊为胰腺癌,进行了新辅助化疗,手术,术后放化疗辅助治疗....然而不幸的是,仅隔一年,M女士的癌症就转移到了肺部,她尝试接受了一种全新的免疫细胞疗法-TILs,仍然无法阻止病情的进展。
2021年6月,M女士的基因检测结果显示她存在KRAS G12D突变,于参加了TCR-T疗法的临床试验。研究人员提取出她的T细胞,在体外进行基因改造,制备出数量巨大的能够特异性识别她体内的KRAS G12D突变癌细胞的TCR-T细胞,再将这支能够精准杀伤癌细胞的T细胞大军回输到M女士体内。
奇迹出现了。一个月后,M女士体内的转移灶开始消退;6个月后,经过评估,M女士的病灶竟然消失了72%!
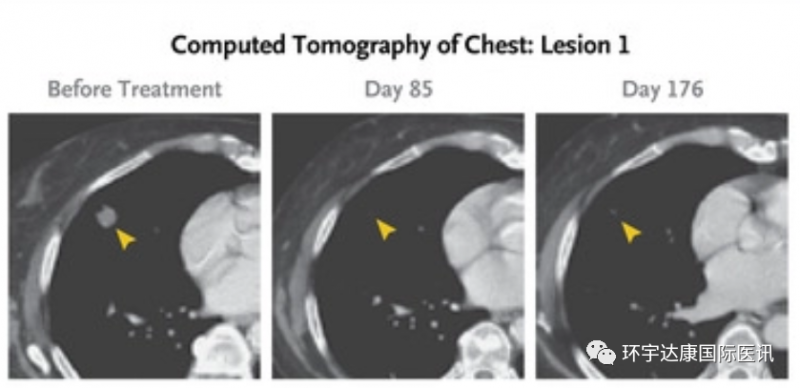
这一研究结果显示,使用TCR-T细胞疗法靶向KRAS G12D突变能够介导转移性胰腺癌肿瘤的消退。另外的好消息是,所有具有这种特定 HLA 等位基因并具有表达 KRAS G12D 突变的肿瘤的患者都可能从这种 TCR 转导疗法中受益,这对于以后治疗表达KRAS G12D胰腺癌及其他实体瘤提供了全新的治疗策略。
注:做了基因检测的病友可以拿出报告看看一旦存在KRAS突变,可以马上联系全球肿瘤医生网医学部看看是否有机会接受国内新药治疗,看不懂的病友也可以致电全球肿瘤医生网医学部解读报告。
什么是TCR-T疗法
相信看完上面的研究,很多病友会问,究竟什么是TCR-T疗法?
人体的免疫防御机制主要依靠体内的白细胞军团,作为白细胞的一种,T细胞有着不可替代的作用,它们是人体里面的特种兵,一旦发现癌细胞,T细胞首先主动出击,杀灭敌人,因此,它也被称为“杀手T细胞”。
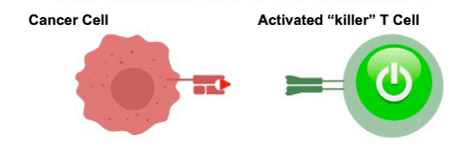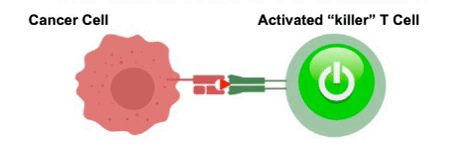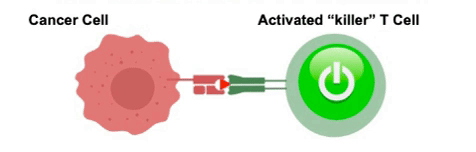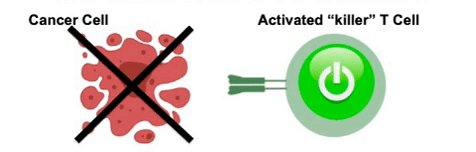
大部分肿瘤患者体内没有足够能识别和杀伤肿瘤细胞的T细胞,对于这些患者,医生可以采用一种称为工程T细胞受体(TCR)治疗的方法。
TCR-T技术,即T细胞受体(TCR)嵌合型T细胞技术,也叫亲和力增强的TCR”技术。它的目的是让自身的杀手T细胞识别能力更强,因为原本的T细胞对肿瘤相关抗原的识别能力较弱,现在通过基因修改的方式增强识别亲和性,从而使T细胞攻击肿瘤细胞,达到治疗肿瘤的效果。
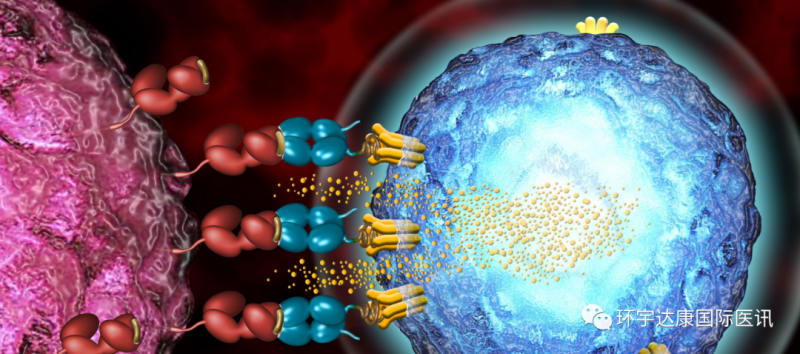
TCR-T疗法需要从患者身上获取T细胞,为T细胞配备新的T细胞受体,使其能够靶向特定的癌症抗原的疗法,这种新型的疗法可以允许医生为每个患者的肿瘤和不同类型的T细胞选择最合适的靶点进行工程改造,使治疗个体化,并为患者提供更大的缓解希望。
与靶向癌细胞表面蛋白的嵌合抗原受体(CAR)修饰的T细胞不同,TCR T细胞疗法能够通过识别与细胞表面免疫相关蛋白结合的蛋白片段,靶向通常在细胞内发现的蛋白。而找到理想的靶抗原是这一技术起效的关键!
比如近两年取得突破性进展的NY-ESO-1、MAGE-A4,这些肿瘤细胞表面抗原都是可以特异性识别识别的。
2022年1月25日,FDA批准tebentafusp-tebn(Kimmtrak,Immunocore Limited),一种双特异性 gp100 肽-HLA 导向的 CD3 T 细胞接合剂,用于 HLA-A*02:01 阳性的无法切除或转移性葡萄膜黑色素瘤。这是全球首款获批的实体瘤TCR-T疗法,这意味着T细胞疗法向实体瘤正式发起挑战,具有里程碑式的意义!
此外,TCR-T 细胞免疫疗法已在部分实体肿瘤的治疗中取得了较好的疗效,特别是对肝癌、黑素瘤、滑膜细胞肉瘤的临床数据都显示出了强大的抗癌活性。相信这一疗法未来将在各类实体肿瘤中开花结果。
宣战实体瘤,众多T细胞疗法临床招募中
目前,基于T细胞的免疫疗法取得了前所未有的突破,目前四大类基于T细胞疗法已问世,好消息是,包括CAR-T,TCR-T,TILs,DC-CTL在内的T细胞疗法,国内正在开展多项临床试验招募癌症患者,想参加的患者可以在线咨询或直接致电全球肿瘤医生网医学部进行进一步评估。
免疫学冰山中蕴藏的生存希望
肿瘤的免疫疗法被誉为攻克癌症的希望,不管是目前已经在众多癌症中获批的PD-1免疫检查点抑制剂疗法,还是以CAR-T为代表的过继性细胞免疫治疗,以及众多如火如荼研发中的癌症疫苗,都只是免疫学冰山中的一角。研究人员正在挖掘冰山中蕴藏的更多信息,如何控制免疫反应,以及将将这些治疗手段用于临床获得益处,给我们越来越多生存的希望,而攻克癌症的希望,或许就在其中。期待免疫疗法取得更多突破,给癌症患者带来更多奇迹。
参考资料:https://www.nejm.org/doi/full/10.1056/NEJMe2204283








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城