CAR-T治疗重磅喜讯,国内首款CAR-T疗法阿基仑赛注射液(抗人CD19 CAR-T细胞注射液)震撼上市,中国迎来细胞免疫治疗元年
太好了!大名鼎鼎的CAR-T疗法终于来到中国了!
提到CAR-T疗法,几乎无人不知,这种有着“治愈”潜力的高精尖技术自2017年在美国上市就另整个医疗界和癌友圈都为之沸腾,引起了巨大的轰动。CAR-T的研发成功,让人们看到了攻克癌症的希望!比如白血病女孩艾米莉已被CAR-T细胞疗法成功“治愈”9年,她也成为这一史诗级疗法的代言人被载入史册。

时隔五年,近日,我们终于迎来了重磅的好消息:2021年6月22日,中国国家药品监督管理局(NMPA)官网显示:复星凯特CAR-T产品阿基仑赛注射液(即抗人CD19 CAR-T细胞注射液)已正式获得批准,在中国正式上市!这是中国上市的首款CAR-T细胞疗法,意味着,中国的肿瘤患者终于迎来了细胞免疫治疗元年!

一,CAR-T疗法阿基仑赛注射液的前世今生
2014年6月,只有19名员工的KITE生物技术公司在美国纳斯达克上市,一天之内狂揽1亿3千万美金!这个小公司没有任何收入,没有一个上市的药物,凭什么如此受投资人的欢迎,而纷纷向它送钱?因为这家公司掌握了一项技术,一项叫CAR-T的技术,一个也许能治愈癌症的技术!
2017 年10 月18 日,KITE生物技术公司的CAR-T细胞药物Yescarta获批上市,用于治疗复发难治性大B细胞淋巴瘤患者,这是美国 FDA 批准的首款针对特定非霍奇金淋巴瘤的CAR-T细胞药物。
随着细胞免疫治疗技术在国际上越来火,中国复兴医药和美国Kite Pharma达成合作,成立复星凯特作为合营公司,以最快的速度将Yescarta产品技术转移至国内。
2018年4月,复星凯特就该产品向国家食品药品监督管理总局提交CAR-T临床试验申请。主要用于复发难治性大B细胞淋巴瘤治疗。
2021年1月12日,复星凯特 CAR-T 细胞治疗产品 FKC876终于“修成正果”,即将在国内上市。这款疗法就是美国的Yescarta(Axicabtagene Ciloleucel),而在我们国内,它有了另一个响当当的名字-阿基仑赛注射液。
2021年6月22日,阿基仑赛注射液在中国正式上市!获批用于二线及以上系统性治疗后复发或难治性大B细胞淋巴瘤成人患者,包括弥漫性大B细胞淋巴瘤(DLBCL)非特指型、原发性纵隔B细胞淋巴瘤(PMBCL)、高级别B细胞淋巴瘤和滤泡淋巴瘤转化的DLBCL。
二,一半以上患者完全缓解!"治愈"血液肿瘤不是梦
2017年10月18日,Yescarta(axicabtagene ciloleucel,前称KTE-C19)在美国震撼上市,用于既往接受二线或多线系统治疗的复发性或难治性大B细胞淋巴瘤(LBCL)成人患者的治疗,包括弥漫性大B细胞淋巴瘤(DLBCL)、原发纵膈大B细胞淋巴瘤(PMBCL)、高级别B细胞淋巴瘤(HGBL),以及源于滤泡性淋巴瘤(FL)的DLBCL(即转化型FL,TFL)。
这款疗法之所以振奋人心,是因为其获批的关键性临床研究ZUMA-1的临床数据显示,YESCARTA对72%的既往治疗失败的晚期非霍奇金淋巴瘤患者有效!其中:51%的患者实现了完全缓解,这意味着一半的晚期患者接受治疗后肿瘤全部消失了;21%的患者出现部分缓解,体内的肿瘤病灶缩小了。
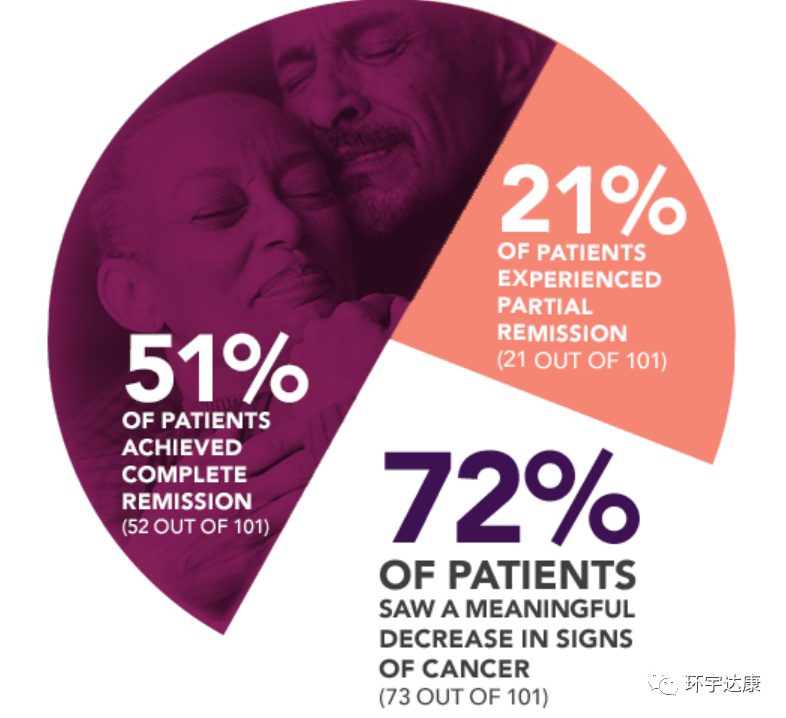
此外,ZUMA-1的长期随访结果显示,随访≥4年,YESCARTA治疗给患者带来了持久的缓解,中位总生存期为25.8个月,4年总生存率为44%,这意味着近一半的晚期难治性患者活过了4年,这款疗法将给国内的患者打开长生寸大门!
三,关于"治愈系"CAR-T疗法
CAR-T疗法全称是Chimeric Antigen Receptor T-Cell Immunotherapy,嵌合抗原受体T细胞免疫疗法。与常规的小分子或生物疗法不同,它是由患者自身的细胞产生。治疗时,患者血液中的T细胞被提取出,经过改造后可表达出嵌合抗原受体,从而识别并攻击表达特定抗原的肿瘤细胞及其他B细胞。简单来说CAR-T技术就如同给你的T细胞装上了GPS导航系统,能识别癌细胞,并进行杀伤,成为免疫军团中的“超级特战队”。

近年来,全球范围内掀起了CAR-T疗法研发的热潮,因为谁先制造出疗效更好、副作用更低的CAR-T治疗技术,毫无疑问将会率先吃到第一只螃蟹,开启肿瘤免疫治疗的新纪元。
目前 ,美国已经批准了五款用于淋巴瘤,白血病,骨髓瘤的CAR-T疗法。其中4款原理均为将患者的T细胞进行基因修饰表达一种旨在靶向抗原CD19的嵌合抗原受体(CAR),CD19是一种表达于多种血液肿瘤细胞表面的抗原蛋白,包括B细胞淋巴瘤和白血病细胞,另外一款靶向BCMA。

四,CAR-T细胞疗法的价格如何
目前,诺华的CAR-T细胞药物Kymriah在美国的定价为47.5万美元(一疗程,下同),Kite的Yescarta定价为37.3万美元。
动辄几百万人民币的治疗费用对于国内普通患者来说,无疑是一笔天价的治疗费用,这也导致CAR-T疗法的患者可及性受到限制。
而自从国内首款CAR-T疗法即将上市的消息公布以来,大家也在猜测和期待国内的价格会不会降低?
据业内人士透露,国内CAR-T商业化落地初期的价格或许与海外定价不会有太大差异。也有专家认为:中国的定价更要符合国情,CAR-T治疗的定价不能参照国外。
那么国外获批CAR-T疗法是如何解决“天价”这一问题的呢?
在美国,在2019年2月批准将CAR-T细胞治疗正式纳入医保;2019年8月,美国医疗保险和医疗补助服务中心(CMS)宣布不仅支付CAR-T细胞疗法的费用,还将支付包括药物管理、细胞的收集和处理、细胞的回输、以及门诊或者住院的所有相关服务与治疗费用。
而作为第一个批准CAR-T疗法的亚洲国家,日本中央社会保险医疗协议会于2019年5月批准将CAR-T细胞治疗产品Kymriah,于5月22日起纳入医保,定价约3350万日元(约合人民币210万元)。纳入医保后,按照日本公共医疗保险的“高额疗养费制度”来计算,使用Kymriah的大部分费用将由日本的公共保险承担,患者最低只需负担41万日元(人民币2.57万元)的药费。且只要是持有合法签证,加入日本医保并按期缴纳费用的外国人也适用。
我们期待,CAR-T疗法在中国上市后,价格能降到人们可承受的范围内,给更多的患者带来“治愈”的机会。
五,弯道超车,中国的CAR-T疗法赶超美国
曾经,这种先进的治疗技术一直掌握在医疗发达国家,很多病友只能苦苦等待国内的临床试验审批等一列流程走完,但是癌症患者真的等不起,有无数的病友们在等待中遗憾离开。这一切终于被改写!
据报道,中国CAR-T细胞研究和临床治疗效果已经追上美国同行!2017年6月,中国(119个注册试验)超过美国(112个注册试验),成为CAR T疗法临床试验最多的国家。截至2020年6月,357个CAR-T试验在中国,在美国有256个试验,58个试验在其他国家,中国CAR-T研究已经处于世界领先水平!
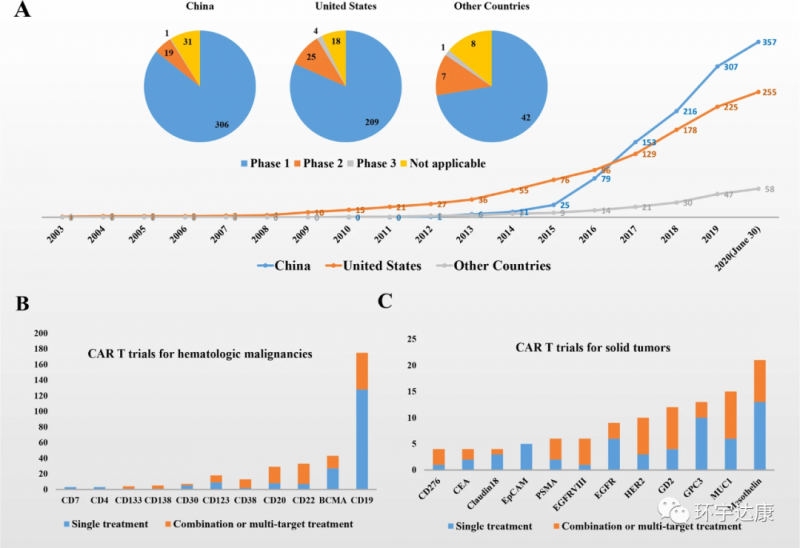
更值得我们骄傲的是,2020年5月,中国自主研发的,世界上第一个针对claudin18.2靶向的CAR-T细胞疗法-CT041获得FDA批准,正式在美国开展临床试验,中国的CAR-T疗法登上世界舞台!
至此,无论血液肿瘤还是实体肿瘤,我们国家都取得了让世界震惊和瞩目的成绩!。CAR-T也被认为是国内企业最有希望跟上全球研发步伐的领域之一!
六,国内患者如何接受CAR-T疗法
目前,距离首款CAR-T疗法正式入市临床应用还有一段时间,并且费用高昂,国内的大部分患者可能还是会面临望药兴叹的窘境。
好消息是,国内已开展多项针对血液和实体肿瘤的CAR-T疗法临床试验,全球肿瘤医生网医学部将重点招募的项目整理出来,给病友们创造更多的治疗和生存机会,符合条件的病友可以申请免费接受这种前沿疗法的治疗。
01、claudin18.2 CAR-T
Claudin18.2(CLDN18.2)是一种胃特异性膜蛋白,被认为是胃癌和其他癌症类型的潜在治疗靶点。基于此,中国研究人员开发了国际上首个针对 Claudin18.2 的 CAR-T 细胞疗法--CT041。
CT041细胞治疗胃癌的临床前研究成果显示,在小鼠模型中可以完全清除胃肿瘤,且没有发生脱靶毒性。
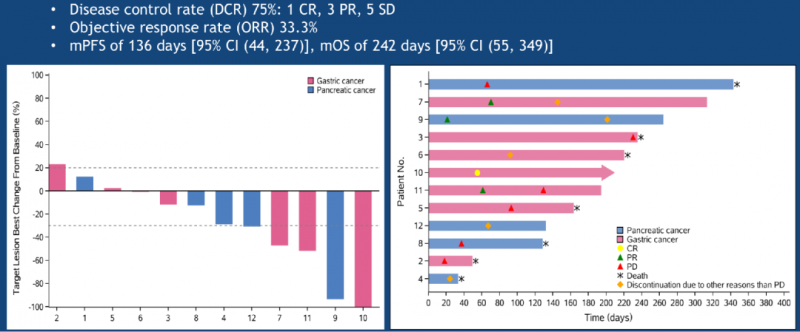
2019 ASCO年会上,一项由北京大学肿瘤医院CAR-Claudin18.2 T 细胞治疗胃癌/胰腺癌的临床数据更新显示,靶向claudin18.2 CAR T细胞治疗12例转移性腺癌(胃癌7例,胰腺癌5例),未发生严重不良事件、治疗相关死亡或严重神经毒性。
11例评估对象中:
1例(胃腺癌)完全缓解;
3例(胃腺癌2例胰腺腺癌1例)部分缓解;
5例病情稳定;
2例病情进展;
总客观缓解率为33.3%。
好消息是,这项试验在2019年正式开展,目前仍由国内胃肠道肿瘤享负盛名的北京大学肿瘤医院胃肠肿瘤科进行临床研究,评估自体人源化抗claudin18.2嵌合抗原受体T细胞在晚期实体瘤中的安全性及功效。
◀招募信息▶
| 疾病 | 治疗 | 阶段 |
| 晚期实体肿瘤(晚期胃癌,食管胃交界癌和胰腺癌) | 药物:CAR-CLDN18.2 T细胞 | 阶段1 |
02、GPC3 CAR-T
除了在研发成功国际上首个靶向Claudin18.2的实体瘤CAR-T疗法。近期,华人团队再次传出好消息:靶向GPC3的CAR-T细胞疗法CAR-GPC3 T细胞治疗晚期肝细胞癌(HCC)的I期临床研究结果出炉,研究结果发表在国际重磅肿瘤学期刊Clinical Cancer Research上,再一次引起轰动。值得一提的是,这是靶向GPC3 CAR T细胞治疗肝细胞癌的全球首个临床试验,华人科学家的研究成果再次在世界舞台闪耀。
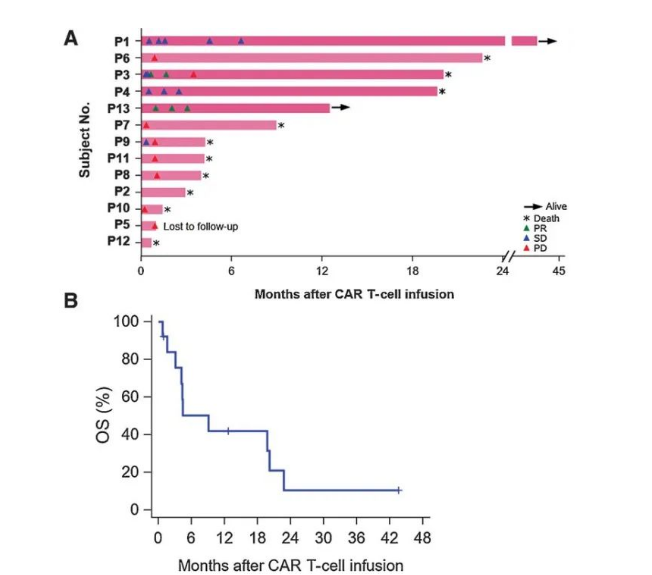
在最新公布的这项研究中,入组了13例晚期肝癌患者(2015年12月至2019年7月24日入组)。
结果显示:
13例受试者中2例获得部分缓解(PR);
3年、1年、6个月生存率分别为10.5%、42.0%和50.3%;
中位生存时间(OS)为278天(95%CI:48,615天)。
GPC3是一种癌胚抗原,参与细胞增殖、分化、迁移和凋亡。正常组织中几乎未见表达,但在70-80%的肝细胞癌中表达。GPC3因其肿瘤特异性,被认为是极有前景的肿瘤免疫治疗靶标。
好消息是,这种新型的CAR-T疗法在国内已正式开始招募患者了。目前由国内几家知名的肿瘤医院率先进行临床研究,评估CAR-GPC3 T细胞疗法在晚期肝癌中的安全性及功效。
入组标准(部分)
1.年龄18至70岁;
2.至少有一个可评估的病灶;
3.标准治疗后进展的患者;
申请流程
1.病理报告,一个月内影像检查资料,近期肝功能报告,近期出院小结电子版或拍照发送至doctor.huang@globecancer.com,邮件中留下联系方式,医学部收到报告分析完毕后一个工作日内电话联系。
2.直接致电全球肿瘤医生网医学部400-666-7998咨询相关医生。
03、间皮素CAR-T
越来越多的临床试验开始尝试将CAR-T用于卵巢癌的治疗,取得了重大突破!我们国内自主研发的一项针对全新靶点间皮素(MSLN)的临床试验已经正式开始招募患者了。
间皮素是细胞表面糖蛋白,在多种肿瘤中高表达,如恶性胸膜间皮瘤、胰腺癌、卵巢癌及部分肺癌,而在正常的胸膜、腹膜以及心包膜表面低表达,因此可以作为理想的靶标,临床前研究表明针对间皮素的CAR-T细胞具有潜在抗肿瘤作用。目前这项临床试验在国内知名的癌症中心进行。
主要入组标准(部分):
1.年龄为18-70岁;
2.细胞学或病理学证实为晚期上皮性卵巢癌(包括输卵管癌和原发性腹膜癌)的女性;
3.影像学检查表明至少有一个可测量病灶。
04、CD20 CAR-T
一项靶向CD20的通用型CAR-T细胞制剂治疗复发难治非霍奇金淋巴瘤的安全性,耐受性 和有效性的单中心临床研究
入组标准(部分):
1.受试者已充分了解参加本研究可能的风险与获益,并且受试者本人或其法定代理人或公正见证人签署知情同意书
2.年龄18-75岁
3.病理学确认的以下复发或难治非霍奇金淋巴瘤类型,CD20阳性或之前曾检测阳性:
– 弥漫大B细胞淋巴瘤(DLBCL)
– 滤泡淋巴瘤(FL)
– 套细胞淋巴瘤(MCL)
– 小淋巴细胞淋巴瘤(SLL)
4.确诊并且有可测量的病灶
05、CD4 CAR-T
一项评价靶向CD4的LCAR-T2C细胞制剂治疗复发/难治CD4阳性 T细胞淋巴瘤患者的安全性,耐受性和有效性的单中心I期临床研究
入组标准(部分):
1.自愿参加临床研究;
2.完全了解、知情本研究并签署书面知情同意书(Informed Consent Form, ICF);
3.愿意遵循并有能力完成所有试验程序• 签署ICF时年龄≥18岁,且≤75岁
4.经研究中心组织病理学确认的 CD4+的外周T细胞淋巴瘤(PTCL):外周T细胞淋巴瘤非特指型(PTCL, NOS)、血管免疫母细胞T细胞淋巴瘤(AITL)、间变性大细胞T细胞淋巴瘤(ALCL)
5.必须至少有1个符合Lugano 2014标准的可评价或可测量病灶
除此之外,CAR-T在实体瘤的特异性靶点,增殖、细胞因子释放等方面已经有了明显改进,国内和国际上还有几百项CAR-T临床研究正在尝试将CAR-T用于实体瘤的治疗,晚期实体肿瘤患者迎来暖春!除了CLAUDIN18.2等,研究人员发现的可用于实体瘤的靶点还有以下几种:
1)Claudin18.2,用于胃癌,胰腺癌等。
2)间皮素(mesothelin),用于治疗间皮瘤、胰腺癌、卵巢癌、肺癌;
3)CEA,用于治疗肺癌、结肠癌、胃癌、乳腺癌和胰腺癌;
4)MUC-1,用于治疗肝癌、肺癌、胰腺癌、结肠癌、胃癌;
5)GPC3,用于治疗肝癌;
6)EGFRvII,用于治疗神经胶质瘤、头颈部肿瘤;
7)B7-H3,用于治疗尤文肉瘤、横纹肌肉瘤、肾母细胞瘤、神经母细胞瘤和髓母细胞瘤以及特别难以治疗的脑干肿瘤(DIPG);
8)PSMA,用于前列腺癌等。
如想了解详情的病友可以致电全球肿瘤医生网医学部进行评估。
申请流程
1.按要求将病历资料提交至全球肿瘤医生网医学部4006667998;
2.医学部初步评估后匹配合适的临床试验;
3.向相应的试验中心提交病历资料;
4.评估通过后协助患者参加临床试验。
CAR-T疗法将给国内患者带来新希望
CAR-T疗法的出现,让更多患者看到部分疾病被治愈的可能。CAR-T疗法也逐步由血液肿瘤向实体瘤进行探索。随着我国鼓励创新,以及更加开放政策的支持下,国内的CAR-T上市步伐也将加快,我们坚信,在完善的细胞免疫监管制度出台后,国家将放开细胞免疫治疗的大门造福更多的癌症患者,我们国家的细胞免疫疗法也将登上国际舞台!








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城