非小细胞肺癌新药,第五款非小细胞肺癌PD1免疫疗法治疗药物Cemiplimab(Libtayo、西米普利单抗)获批一线
2021牛年刚刚开启,国内外新药井喷上市的好消息接连不断!
2021年2月18日,FDA宣布对首个挑战KRAS的革命性新药Sotorasib优先审批,将于2021年8月前上市;
2021年2月19日,全球首款鼻咽癌免疫疗法,我国自主研发的PD-1特瑞普利单抗注射液获批上市。
刚刚,FDA再传捷报!2021年2月22日,FDA批准PD-1疗法cemiplimab单药一线治疗PD-L1表达>50%的晚期非小细胞肺癌患者。这意味着,非小细胞肺癌迎来了第五款免疫检查点抑制剂,cemiplimab成功冲进免疫单药一线治疗肺癌,晚期患者迎来了“去化疗”新时代!
Libtayo进军肺癌一线治疗!晚期肺癌迎来"去化疗"时代
FDA此次批准是基于代号为EMPOWER-Lung 1的III期试验数据。
在2020年ESMO大会上公布的最新结果显示,对于晚期非小细胞肺癌(NSLSC)的患者,尤其PD-L1高表达的患者,当Libtayo(cemiplimab)作为一线治疗时,与铂类化疗相比,可显着延长总体生存期和无进展生存期。
实验设计:
这项III期临床试验纳入了710名晚期非小细胞肺癌患者,这些患者均为无法手术或化疗,或者化疗后进展,以及未经治疗的转移性非小细胞肺癌患者,其中还有10%的患者癌症已经扩散到大脑。将患者随机分配至铂类化疗组和Libtayo组。主要终点为总生存期和无进展生存期(PFS)。
试验结果:
在563名PD-L1表达水平≥50%的患者中,Libtayo将死亡率降低了43%,此外,疾病进展的风险降低了46%,PFS时间分别为8.2个月和5.7个月。总缓解率为39%vs20%。
值得一提的是,Libtayo的总体缓解率与PD-L1表达密切相关。在PD-L1表达水平≥90%的缓解率为46%。大约六个月后,肿瘤消退了40%以上。因此,确诊为非小细胞肺癌患者的患者快去检测下PD-L1,一旦高表达可优先考虑使用这款免疫检查点抑制剂。
安全性:
治疗通常是安全的,贫血,疲劳,肺炎,食欲下降,便秘和恶心是最常见的不良反应。
Libtayo的上市,将给PD-L1高表达的晚期非小细胞肺癌患者带来无需化疗的新选择。另外一个好消息,在中国,cemiplimab也已经获批开展临床试验,与含铂化疗联用或单药一线治疗晚期或转移性NSCLC患者。一旦开始招募,全球肿瘤医生网医学部将及时公布招募信息。
关于Libtayo,肺癌患者要了解的五个问题
01、LIBTAYO药品信息
商品名:LIBTAYO
英文名:cemiplimab
中文名:西米普利单抗
生产厂家:赛诺菲&再生元
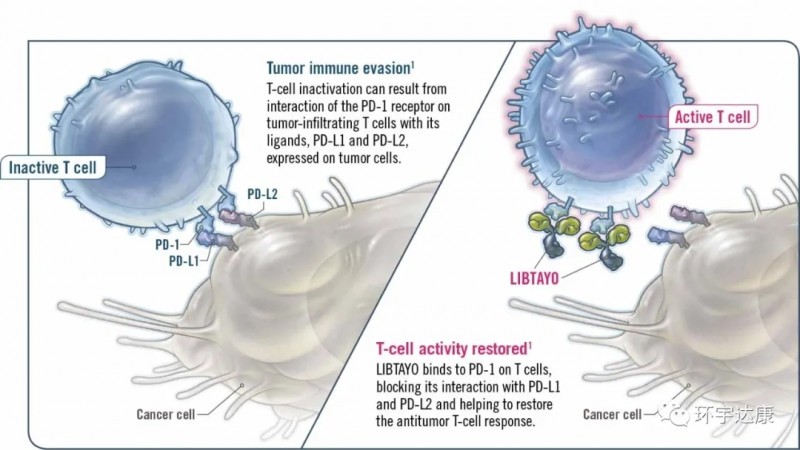
LIBTAYO(cemiplimab 西米普利单抗)是一款针对PD-1靶点的单克隆抗体药物。通过特异性的与PD-1结合,LIBTAYO能够“破除”癌细胞对于T细胞的抑制,T细胞受体信号可以重新激活,恢复抗肿瘤活性,增强人体免疫系统对于癌细胞的杀伤能力,达到抗癌的效果。
2018年,LIBTAYO首次获批用于治疗皮肤鳞状细胞癌。
02、哪些非小细胞肺癌患者可以使用Libtayo
Libtayo获批的适应症为:单药一线治疗PD-L1表达>50%的晚期非小细胞肺癌患者。因此,晚期非小细胞肺癌患者确诊后需要及时做PD-L1检测和基因检测,如果表达高于50%,并且没有EGFR,ALK,ROS1等其他基因的突变,可以优先考虑使用Libtayo。
03、治疗需要多长时间
如果治疗持续有效,目前的研究证据支持在持续治疗2年后停药。
04、常见副作用有哪些
常见副作用:乏力、输注相关反应、腹泻、结肠炎、肝毒性、肺炎、自身免疫性甲状腺疾病(甲减、甲亢)垂体炎、肾上腺功能减退症、1型糖尿病、急性肾损伤、淀粉酶及脂肪酶升高等。
05、除了Libtayo,还有哪些PD-1/L1获批用于非小细胞肺癌
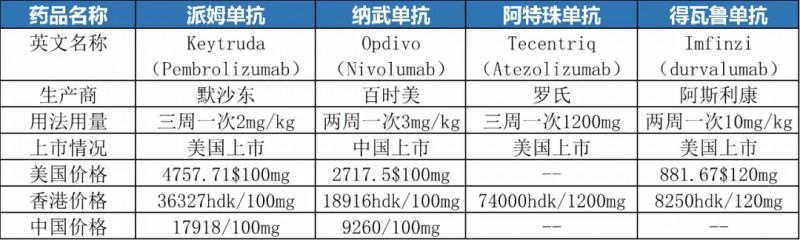
目前除了刚刚获批的Libtayo,还有四款PD-1/L1获批用于非小细胞肺癌:Pembrolizumab(帕博丽珠单抗),nivolumab(纳武利尤单抗),atezolizumab(阿特朱单抗),durvalumab(得瓦鲁单抗),将晚期肺癌不到5%的五年生存率大大提升。免疫疗法正在逐渐成为治疗晚期非小细胞肺癌的“特效”药物。
图片3
免疫治疗不断刷新晚期NSCLC患者的生存时间,真正可能使NSCLC变为慢性病。但目前免疫治疗还有很多问题需要解决,比如探寻更佳、更多的生物标志物指导精准选择人群;免疫治疗合理的持续时间;联合治疗方式的选择、顺序的选择、剂量的选择等等,我们期待有更多的免疫疗法能够获批上市,给病友们带来更多的治疗选择和希望。目前,免疫疗法在国内开展的多项临床试验正在招募患者,想申请的患者可以将基因检测报告,病理报告提交至全球肿瘤医生网医学部4006667998进行初步评估,我们的专家将为您全面分析检测报告,匹配能够入组的临床试验,以及有无新药可以使用。)
注:请将基因检测报告,诊断报告电子版或拍照发送至doctor.huang@globecancer.com,邮件中留下联系方式,医学部收到报告分析完毕后一个工作日内电话联系。
参考资料:
https://www.onclive.com/view/fda-approves-cemiplimab-for-frontline-advanced-nsclc-with-high-pd-l1-expression








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城