早期乳腺癌新辅助放疗VS早期乳腺癌辅助放疗|基于人群的超大样本研究
导读
早期乳腺癌的标准治疗方案为保乳术/改良根治术+淋巴结活检/清扫,序贯瘤床和全乳的辅助放疗。辅助放疗显著减少了乳腺癌的复发风险。对于腋窝淋巴结阳性,或T3-4肿瘤来说,需要进行术后的胸壁+腋窝淋巴结放疗。
在局部进展期乳腺癌中,术前新辅助放化疗可以达到使不可手术患者降期,提供手术机会的作用。最近有研究表明,由于CTV较小,接受新辅助加速部分乳腺照射(APBI)可以明显减小患者的软组织毒性。但是目前,尚没有基于人群的,关于新辅助放疗的长期疗效研究公布。
所以,来自美国的研究团队开展了一项研究,对比辅助放疗、新辅助放疗在早期乳腺癌患者中对总生存(OS),无肿瘤生存(CFS)的差异。该研究于近期发表在了Breast Cancer Research上。
主要内容
该研究团队搜索了美国1972年-2012年SEER、NCI数据库中,接受手术和局部放疗的原发性乳腺癌患者。入组患者全部为女性,原位癌或T1-T3,被分至两组:新辅助放疗序贯手术组和手术序贯辅助放疗组。
探究接受辅助放疗和新辅助放疗患者生存预后的区别。研究终点包括CFS和OS。(CFS定义:从第一次确诊肿瘤的日期至确诊第二原发肿瘤的时间)
主要结果
该研究团队通过COX分析发现,辅助和新辅助放疗的队列在ER状态、手术方式等等不同时分布明显存在差异,所以该研究针对ER状态和手术方式进行了分层(图1)。
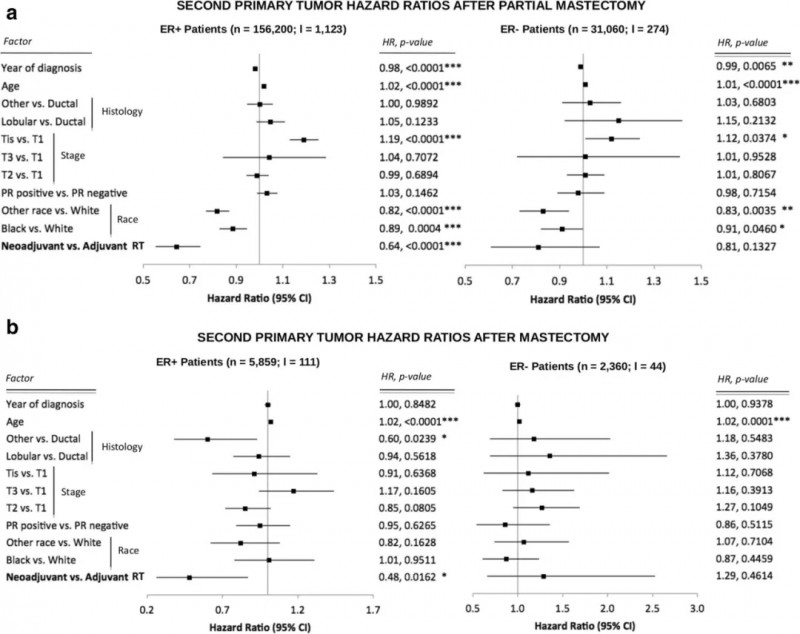
结果表明在ER阳性亚组中,接受新辅助放疗患者的CFS显著低于接受辅助放疗的患者(HR 0.64, p<0.0001; 保乳术亚组:HR, 0.64, p<0.0001; 根治组:HR, 0.48, P=0.0162)(图1)。
保乳手术的患者,如果诊断、治疗年份靠后,其发生二次原发肿瘤的概率稍微减小(HR≤0.99, p<0.01)。
有趣的是,原位癌患者接受保乳手术相比于T1肿瘤患者来说,发生第二原发肿瘤的概率要明显增大(ER阳性:HR 1.19, p<0.0001; ER阴性:HR, 1.12, P=0.0374)。
在ER阳性患者、保乳术这一最大的队列(n=155,077)中,接受新辅助治疗的HR要较接受辅助治疗的HR高出12%(0.75 vs 0.63; p<0.0001)(图2a)。
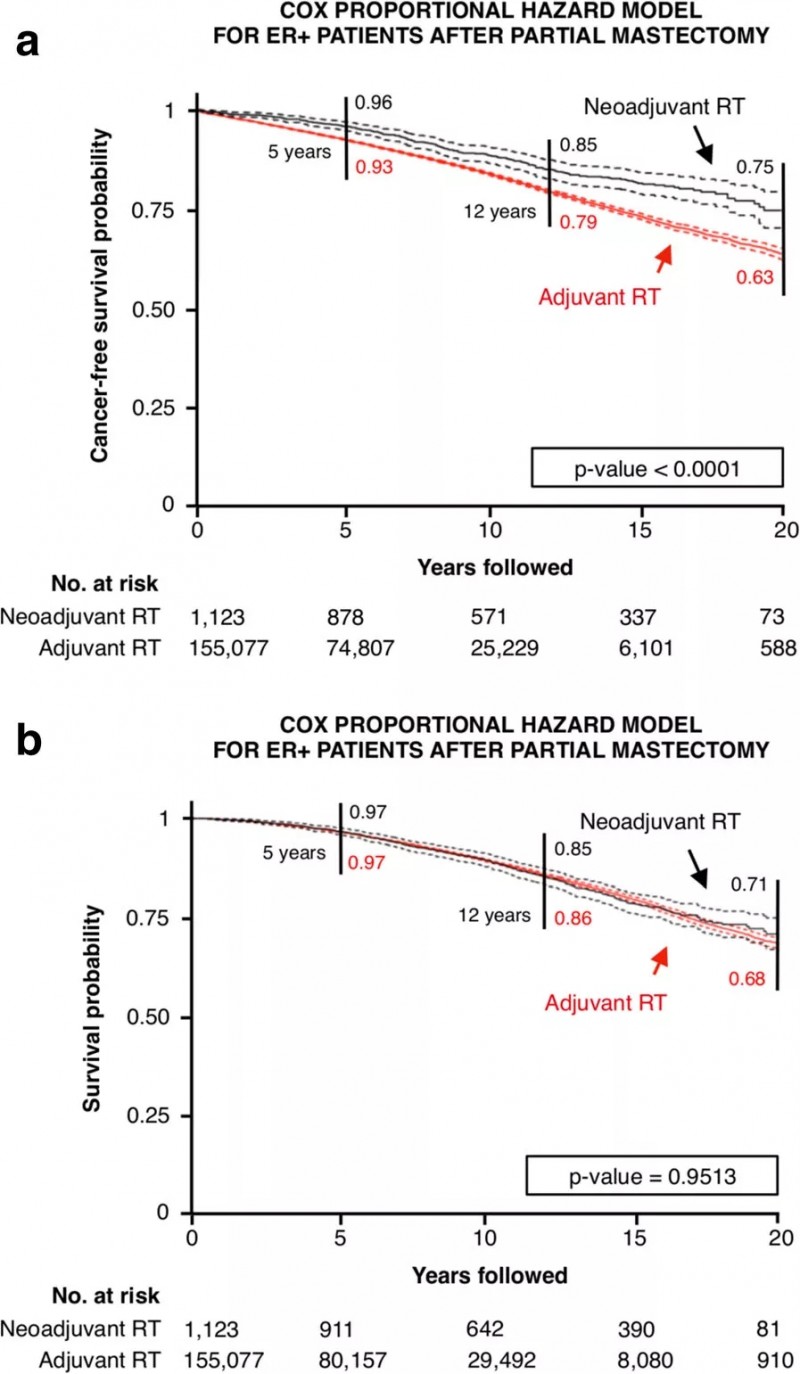
总生存期(OS)方面,接受辅助、新辅助治疗患者的中位随访时间为7年和16.3年,最大分别为38.9年和38.6年。
COX分析发现,ER状态、术式等因素也影响了患者的生存期,需要进一步分层。但是,新辅助治疗组的患者病例数却不够,导致了多因素分层分析无法进行。
总体来看,新辅助治疗 vs 辅助治疗的早期乳腺癌患者,虽然CFS有明显差别,但是死亡率却几乎相同,两组的OS曲线直到第20年随访时仍无法分开(HR, 1.00; P=0.9513)(图2b)。
但是,除了ER状态、术式之外,肿瘤分期、年龄、种族等等因素也都影响了患者的死亡率。
小结
该基于人群的研究最终的结论为,对早期乳腺癌患者,尤其是ER阳性的患者来说,术前接受新辅助放疗与术后辅助放疗相比,患者的第二原发肿瘤发生率会有所升高。
但是,总体来看新辅助放疗与辅助放疗相比,却未升高早期乳腺癌患者的死亡率。
这些发现对于进一步探究新辅助放疗的作用十分重要,急需前瞻性数据对比新辅助、辅助放疗患者的远处转移率和局部控制,以确定新辅助放疗的地位。
另外,另一有趣的发现是原位癌患者较T1肿瘤患者相比,接受保乳手术可导致患者CFS的上升。所以原位癌患者可能更不适合接受保乳手术治疗,期待进一步的探索和数据支持。
参考文献
Poleszczuk J, Luddy K, Chen L, et al. Neoadjuvant radiotherapy of early-stage breast cancer and long-term disease-free survival[J]. Breast Cancer Res, 2017,19(1):75. DOI: 10.1186/s13058-017 -0870-1.
文章来源:医脉通 医脉通肿瘤科








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城