广谱抗癌药,广谱靶向药,拉罗替尼临床试验和恩曲替尼临床试验国内招募正式开始
近两年,除了免疫检查点抑制剂在肿瘤医患群体中成为焦点,其中KEYTRUDA更是成为首款不区分癌症种类和来源的广谱抗癌药,开启了肿瘤治疗的新时代,另外两款TRK抑制剂Vitrakvi&Rozlytrek也大放异彩,被誉为“无进展生存系”的传奇抗癌药,成为癌症疗法从“基于癌症在体内的起源”转向“基于肿瘤的遗传特征”这一演变过程中的重要里程碑。
这两款不分癌症种类的广谱抗癌药开启了肿瘤治疗的新篇章,具有划时代的意义,那么这两款广谱抗癌药究竟有哪些不同,病友们究竟该如何选择呢?下面是这两款药物全面的用药信息对比,包括适应症,无进展生存率,副作用,用法用量,价格全面对比,希望在抗癌的道路上能给大家提供更多的希望和帮助。
Vitrakvi&Rozlytrek用药信息大盘点
| 药品名称 | 代号 | 生产厂家 | 作用靶点 | 上市时间 | 适应症 | 临床效果 | 规格及价格 | 使用剂量 | 副作用 |
| 拉罗替尼(Larotrectinib、Vitrakvi) | LOXO-101 | 罗氏 | NTRK | 2018.11.26 | 治疗患有NTRK基因融合的局部晚期或转移性实体瘤的成人和儿童(12岁以上) |
NTRK融合阳性实体瘤成人患者:75% NTRK融合阳性实体瘤儿童患者:93% NTRK融合阳性非小细胞肺癌患者:4例接受拉罗替尼治疗的NTRK基因融合的NSCLC患者中的3例都出现持续反应(从8.21到>20.27个月) |
成人口服胶囊25mg和100mg,每月32800美元(30天100mg) 儿童患者为口服液体制剂,每月1.1万美元 |
成人:对成年人的剂量是每天口服100mg,每天两次,直至疾病进展或出现不可接受毒性 儿童:按年龄和体重使用剂量:体表面积小于1.0米的儿科患者,推荐剂量是100mg/m2,每日口服两次,与或不与食物同服 |
疲劳、恶心、头晕、呕吐、AST升高、咳嗽、ALT升高、便秘和腹泻。 警告神经毒性、肝毒性和胚胎胎儿毒性。 |
| 恩曲替尼(Entrectinib、Rozlytrek) | RXDX-101 | 拜耳 | NTRK/ROS1/ALK | 2019.8.16 |
1.治疗NTRK基因融合阳性的晚期复发实体瘤的成人和儿童患者 2.ROS1阳性非小细胞肺癌(NSCLC)患者 |
NTRK融合阳性实体瘤成人患者:57.4% NTRK融合阳性实体瘤儿童患者:100% 局部晚期或转移性ROS1阳性非小细胞肺癌(NSCLC)患者:总缓解率达到78.8%,完全缓解率达到5.9% |
口服胶囊100/200mg,每月17050美元 |
成人:在成人中的推荐剂量是每天口服600mg,与或不与食物同服,知道疾病进展或不可及受的毒性 12岁以上儿童: 体表面积: 大于1.50 m2使用600mg 1.11-1.50m2使用500mg .091-1.10m2使用400mg |
疲劳、恶心、头晕、呕吐、咳嗽、便秘和腹泻、味觉障碍、水肿、感觉迟钝、呼吸困难、肌痛、认知障碍、体重增加、发热、关节痛和视力障碍。 警告肝毒性和胚胎-胎儿-以及充血性心力衰竭、中枢神经系统效应、骨骼骨折、高尿酸血症、QT间期延长和视力障碍 |
两大广谱抗癌药Vitrakvi&Rozlytrek国内招募正式开始
拉罗替尼(Larotrectinib)和恩曲替尼的上市无疑给很多晚期患者带来了全新的选择和希望,但,目前国内均未上市。
国内患者只能选择出国购买,但费用高昂,以拉罗替尼为例,每瓶售价超过23万元人民币,再加上诊断、交通等费用,大部分患者只能汪洋兴叹。
如果说有什么比“无药可治”更让人绝望的,那就是有特效药,但却买不到!买不起!
去年,拉罗替尼和恩曲替尼将在国内开展临床招募的信息公布后,引起了广泛的关注。终于,经过半年多的审批流程,拉罗替尼和恩曲替尼这两款不限癌种的广谱抗癌药双双宣布好消息,在中国正式招募患者!这意味着,国内的患者也终于有机会免费用上这些美国的抗癌“特药”!
这些实验是国际多中心的试验,中国也参与了,由国内肿瘤领域的几家医院率先开展。
一,恩曲替尼成人实体瘤招募信息
这项 Entrectinib治疗携带 NTRK1/2/3、ROS1或 ALK基因重排的局部晚期或转移性实体瘤患者的开放性、多中心、全球性 II期篮式研究,来确定携带NTRK1/2/3、ROS1或ALK基因重排的每类实体瘤患者人群(篮子)接受Entrectinib治疗后的客观缓解率(ORR)。
试验分类:安全性和有效性
试验范围:国际多中心试验
试验分期:II期
主要终点指标:由独立放射学审查委员会测定 总缓解率
入组条件(部分):
1. 经组织学或细胞学确诊为局部晚期或转移性实体瘤,而且根据Foundation Medicine, Inc.或CLIA认证或同等机构认可的当地诊断实验室采用任何核酸类诊断检测方法进行的检测,该肿瘤携带一种预计分别转化成具有一个功能性TrkA/B/C、ROS1 或ALK激酶结构域的融合蛋白的NTRK1/2/3、ROS1或ALK基因重排,且不同时存在第二种致癌因素(例如EGFR、KRAS);
2. 对于通过当地实验室分子检测入组的患者,要求提交存档或新鲜的肿瘤组织(除非存在医学禁忌),在Foundation Medicine, Inc.或该地区其他认可的中心实验室进行独立中心分子检测;
3. 根据当地采用RECIST v1.1进行的评估,疾病可测量。

二,拉罗替尼成人实体瘤招募信息
这项研究是为了验证拉罗替尼对不同类型的肿瘤疗效。这些肿瘤必须存在一种特定的基因变化(NTRK1, NTRK2或NTRK3)。Larotrectinib是一种试验性的药物,可以阻止这些NTRK基因在癌细胞中的作用,因此可以用来治疗肿瘤。
试验分期:II期
主要终点指标:由独立放射学审查委员会测定 总缓解率
入组人数:总体140人中国13人
预计入组结束时间:中国2021年8月31日
| 序号 | 机构名称 | 首席研究员(PI) | 城市 |
| 1 | 中山大学附属肿瘤防治中心 | 徐瑞华 | 广州 |
| 2 | 复旦大学附属中山医院 | 刘天舒 | 上海 |
| 3 | 四川大学华西医院 | 刘咏梅 | 成都 |
| 4 | 北京大学肿瘤医院 | 沈琳 | 北京 |
三,拉罗替尼儿童实体瘤招募信息
本研究是验证拉罗替尼在儿童肿瘤患者中的安全性。该肿瘤必须存在特定(NTRK)基因改变。拉罗替尼旨在限制肿瘤细胞中NTRK基因的活性而治疗肿瘤。研究的第一部分(I期)验证儿童受试者中,剂量的安全性,药物在体内的吸收和改变,对于肿瘤的作用。第二部分(II期)主要目的是药物治疗的作用及其时长。
主要终点指标:1期:受试者发生不良事件的例数,不良事件持续的时间;II期由独立放射学审查委员会测定 总缓解率。
入组人数:国际多中心试验:总体159人中国5人
预计入组结束时间:中国2021年11月30日
| 序号 | 机构名称 | 首席研究员(PI) | 城市 |
| 1 | 中山大学附属肿瘤防治中心 | 徐瑞华 | 广州 |
| 2 | 天津市肿瘤医院 | 赵强 | 天津 |
| 3 | 北京儿童医院 | 王焕民 | 北京 |
哪些患者可以申请临床试验
相信拉罗替尼和恩曲替尼在国内临床试验的开展,无疑让山重水复疑无路的晚期患者多了一份希望,但是想使用这两款“无进展生存系”神药有个硬性条件,必须通过基因检测证实存在NTRK1、NTRK2或NTRK3融合基因的局部晚期或转移性恶性肿瘤。注意只能是融合,NTRK突变或扩增都不适合。
如果说这两款广谱抗癌药是一把锁,NTRK基因就是打开这把锁的“生命之钥”,只要有NTRK的融合,相当于是打开了通往无进展生存之路的大门。
然而这把钥匙却像钻石一样珍贵,不是每个患者都能获得的。
首先是因为它非常罕见,在中国常见的肺癌,乳腺癌,结直肠癌中,只有1%~5%的患者存在这种突变,而一些罕见的癌症,比如婴儿纤维肉瘤和分泌型乳腺癌,存在NTRK融合的频率却高达90%~100%。其次,这款药物对所有存在NTRK融合突变的患者通常都能快速起效,很多晚期患者在使用拉罗替尼后得到了重生,像钻石一样罕见又珍贵。

NTRK(NeuroTrophin Receptor Kinase)是神经营养因子受体络氨酸激酶,包含NTRK1、NTRK2和NTRK3,这个基因如果和其他的基因发生了融合突变,那么就导致了异常的活性,驱动了肿瘤的发生,比如目前,婴儿纤维肉瘤,先天性中胚层肾病和分泌性乳腺癌都显示出ETV6-NTRK3融合,就是ETV6和NTRK3基因发生了融合,以及一些肉瘤中出现的TPM3-NTRK1,就是TPM3和NTRK1基因发生了融合。

除了拉罗替尼(Larotrectinib)是第一款FDA批准的不分年龄和癌种类型针对NTRK融合的广谱TRK抑制剂,关于这个靶点的治疗,近两年是肿瘤领域除了免疫检查点抑制剂之外的另一个研发热点,比如2019年刚上市的恩曲替尼,以及针对一代LOXO-101耐药研发的二代NTRK抑制剂loxo-195,都是抑制酪氨酸激酶的活性!
NTRK临床治疗案例
案例一
克里斯蒂娜·洛瑞(Christina Lowry)说:“最开始我们以为她被虫子咬了,但结果却是一种低分化的梭形细胞肉瘤。
医生说,因为肿瘤被包裹在气管和肺部主要血管周围,并且一部分肿瘤还侵犯了米歇尔的神经,导致她的上臂和面部无力。所以无论如何,手术是不可行的。
当时,Leo Mascarenhas博士正在进行一项新药临床试验,叫做larotrectinib的口服药物。这个药物是专门针对表达NTRK融合蛋白的肿瘤,这是一种由两个独立的基因组成的杂交癌基因,可以驱动肿瘤的生长。他非常怀疑米歇尔的肿瘤可能带有NTRK融合蛋白,因此让检测公司要求加快分子检测的速度。结果惊喜的发现,米歇尔的肿瘤真的存在TPM3-NTRK1融合。医生兴奋的说,这根关键的救命稻草简直出现的太及时!因为存在这个突变意味着米歇尔可能有资格参加专门针对NTRK融合的新药物larotrectinib的临床试验。

整个过程快到超乎想象,仅在米歇尔的基因检测报告出来后的17个小时,米歇尔就接受了第一次治疗,而这个过程通常最快也需要1~2周,每个人都在拼命的将米歇尔从死神手中抢回来。
入组后,他们遇到的第一个问题就是用药。因为临床试验药物存储在专门的研究药房中,该药房仅在工作日开放,在了解了米歇尔的病情后,实验小组开了绿灯,一名研究药剂师专门在周六为米歇尔准备了她需要的每日两次的悬浮液剂量,用注射剂让米歇尔缓慢喝下。

而让医生震惊的是,米歇尔仅仅在治疗后的24小时内,就对药物做出了响应,症状迅速好转,这远远超出了医生的预期,周六来医院的时候她还在重症监护室,而周二,她就和爸爸妈妈回家了,他们抓住最后一根救命稻草,这简直是个奇迹!
治疗两个月后,第一次扫描发现她的肿瘤已经缩小了约60%,放射科的医生说肿瘤已经小的很难进行测量了,米歇尔会继续接受治疗直到她对药物耐药或肿瘤完全“滚蛋”为止。
基于米歇尔和其他临床数据的惊艳结果,美国FDA已经于2018年11月26日正式批准了larotrectinib上市!
故事更新:2019年11月消息: 米歇尔的肿瘤现在缩小到在她最近的3场MRI扫描中都无法检测到的程度。米歇尔(Michelle)的父亲乔(Joe)说:“当米歇尔人生的旅程重新开始时,我们希望她每一天都有最好的生活。

案例二
2013年的一个艳阳天,一个抽了30年烟的45岁大叔迎来晴天霹雳,IV期肺腺癌。他的双肺都有肿瘤,胸壁上还有一个用手都可以摸得到的5厘米的肿瘤;更糟的是,CT显示他的脑部已经有有15-20个左右的转移灶(有些太小了,有的连在一起,具体多少个数不清楚了,还未出现临床症状),做了肺癌常见的EGFR、ALK、ROS-1、C-MET、RET基因检测后,都没有突变……
他开始尝试四种不同的方案,卡铂+培美曲塞、长春瑞滨、多西他赛)以及救活了美国总统的逆天“神药”PD-1(keytruda),然并卵,病情继续恶化……
在主治医生的建议下,他做了全基因组测序,终于发现了一个罕见的突变(阳性率大约是千分之一):SQSTM1-NTRK1突变。

那个年代,国内估计还没几个人知道这个基因,它是NTRK家族基因重排中的一种,NTRK基因目前已经发现的有3个,NTRK1、NTRK2、NTRK3。
当时在国内外都还没有针对这个靶点的药物上市,但是美国就是好啊,新药研发就是多啊,大叔很幸运的入组了针对这类突变的新药Entrectinib(小名叫做:RXDX-101,中文名恩曲替尼)的临床试验。
接下来就是见证奇迹的时刻:
大叔每天以400 mg / ㎡口服,三周后,疼痛和呼吸困难症状消失,不在需要吸氧,并且,全身的肿瘤缩小46%,胸壁5公分的病灶已看不到摸不到!脑部肿瘤大部分消退;吃药5个月,症状不断改善,全身的肿瘤缩小77%,脑转移完全消失!!!
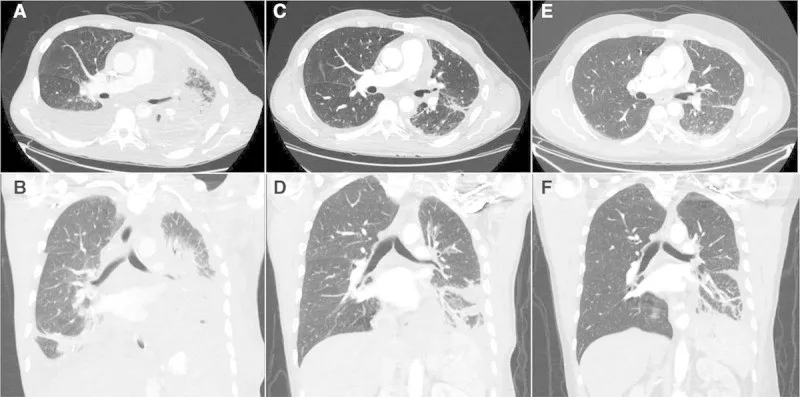
第26天(C,D)和第155天(E,F)胸部图像,肿瘤缩小77%!

吃药前箭头指的都是肿瘤,20几个,吃药26天(DF)大部分消失, 吃药155 天(GI)肿瘤完全消失!
案例还有很多,不在此一一列列举了。就像LOXO-101和PD-1,我们希望这些广谱的抗癌药能尽早在国内上市,进入医保,造福更多的癌症患者!








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城