肺癌新药,肺癌免疫治疗药物,肺癌PD-1治疗药物百泽安(替雷利珠单抗注射液)获批肺癌一线治疗
近两年,免疫治疗可谓是遍地开花。而怀揣梦想、探索肿瘤治疗的中国制药企业也为了展现中国风采,将多个国产PD-1/PD-L1单抗推上世界舞台。
在同类药物中,百济神州(BeiGene)旗下的PD-1抗体药物替雷利珠单抗注射液(商品名:百泽安®)可谓是一骑绝尘,不仅在2019年12月27日获得国家药品监督管理局(NMPA)批准用于治疗至少二线系统化疗的复发或难治性经典型霍奇金淋巴瘤(R/R cHL)患者,更是在2020年4月9日,被NMPA批准用于治疗接受含铂化疗失败(包括新辅助或辅助化疗12个月内进展)的局部晚期或者转移性PD-L1高表达的尿路上皮癌(UC)患者。
目前在全球范围内,已经有10款PD-1/PD-L1疗法获批,其中已有8款在中国获批,这10款疗法中,已有6款获批尿路上皮癌适应症。值得一提的是,替雷利珠单抗是国内首个被批准治疗尿路上皮癌的PD-1单抗。

图为6款获批尿路上皮癌适应症的PD-1/PD-L1药物
客观缓解率24.8%,开启晚期尿路上皮癌治疗新篇章
此次获批基于替雷利珠单抗治疗尿路上皮癌的II期临床研究——BGB-A317-204研究,共入组113例既往接受过含铂化疗的PD-L1阳性的局部晚期或转移性尿路上皮癌患者,主要疗效终点为客观缓解率(ORR)。
在最后可评估的101例患者中,10例患者完全缓解(CR为9.9%),15例患者部分缓解(PR为14.9%),客观缓解率(ORR)为24.8%,疾病控制率(DCR)为38.6%。亚组分析表明,缓解率受基线因素影响不大,不同基线情况患者均可出现临床缓解。
整体的无进展生存期(PFS)为2.1个月,中位总生存时间(OS)达到9.8个月,相比过往的治疗,疗效有很大的进步,取得了不错的治疗效果。此外,替雷利珠单抗联合化疗一线治疗尿路上皮癌的III期临床研究也已经启动。
总控制率高达91%,一线治疗非鳞肺癌获得成功!
百济神州4月14日宣布,评估抗PD-1疗法百泽安(替雷利珠单抗注射液)联合培美曲塞(pemetrexed)及铂类化疗一线治疗非鳞状非小细胞肺癌(NSCLC)患者的III期临床试验达到了主要终点。在一项计划的中期分析中,经独立评审委员会(IRC)评估,与培美曲塞+铂类化疗治疗组相比,百泽安®+培美曲赛+铂类化疗治疗组无进展生存期(PFS)取得了统计学意义的显著提高。
百济神州已计划与国家药品监督管理局药品审评中心(CDE)讨论,递交百泽安用于一线治疗非鳞状非小细胞肺癌新适应症的补充新药申请,并计划在未来召开的医学会议上公布详细的试验数据。
根据2019年CSCO公布的结果显示:替雷利珠单抗联合化疗一线治疗的总疾病控制率(DCR)高达91%,在67%的患者(n=36)中观察到确认的客观缓解率(ORR),非鳞状非小细胞肺癌组、鳞状非小细胞肺癌队列A组(替雷利珠单抗联合紫杉醇与铂类)、鳞状非小细胞肺癌队列B组(吉西他滨与铂类)、小细胞肺癌组的ORR分别为44%、80%、67%、77%。

从2017年7月起入组,截至2019年2月25日,供纳入54例患者,中位治疗时间为9.6个月,14例(25.9%)患者目前仍在接受治疗。
此外,研究数据显示替雷利珠单抗联合化疗治疗晚期肺癌患者整体耐受性良好,相关的不良反应以轻、中度为主,≥3级不良反应发生率占9.3%,导致治疗终止的不良反应发生率低。
PD-1抗体替雷利珠单抗,抗肿瘤活性威力不可小觑
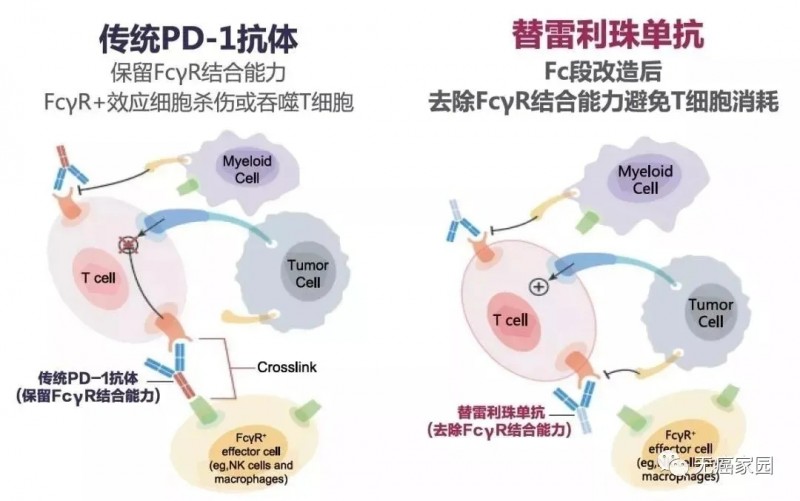
那么,替雷利珠单抗到底相比传统PD-1到底具备哪些优势呢?这不得不提其独特的药物结构,在传统PD-1抗体的基础上,替雷利珠单抗进一步优化了分子结构,具有区别于传统PD-1抗体的独特结合表位,通过基因工程改造,替雷利珠单抗可避免与FcγR结合,从而消除了抗体依赖的细胞介导的吞噬作用(ADCP),避免了因T细胞数量减少而影响抗肿瘤疗效,这使得替雷利珠单抗的抗肿瘤活性更高。
此外,替雷利珠单抗还具有优异的结合动力学表现,对PD-1具有更高的亲和力,分别比纳武利尤单抗和帕博利珠单抗高约50倍与40倍,并且从PD-1上解离的速率放缓了约50倍和100倍,使得疗效更为持久。
除了上述已获批的适应症之外,替雷利珠单抗正作为单药疗法及联合疗法开发针对一系列实体瘤和血液肿瘤治疗适应症,包括非小细胞肺癌、小细胞肺癌、肝癌、食管癌、胃癌、尿路上皮癌等。








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城